为测定某有机化合物A的结构,进行如下实验。
Ⅰ.分子式的确定
(1) 将有机物A置于氧气流中充分燃烧,实验测得:生成5.4gH2O和8.8gCO2,消耗氧气6.72L(标准状况下)。则该物质分子中碳、氢、氧原子个数比为
(2) 质谱仪测定有机物A的相对分子质量为46,则该物质的分子式是
(3) 根据价键理论,预测 A的可能结构并写出结构简式
A的可能结构并写出结构简式
Ⅱ.结构式 的确定
的确定
(4) 核磁共振氢原子光谱能对有机物分子中不同位置的氢原子给出不同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目。
例如:甲基氯甲基醚(Cl—CH2—O—CH3)有两种氢原子(图1)。经测定,有机物A的核磁共振氢谱示意图(图2),则A的结构简式为 。
Ⅲ.性质实验
(5) A在一定条件下脱水可生成B,B可合成包装塑料C。体育比赛中当运动员肌肉扭伤时,队医随即用氯乙烷(沸点为12.27℃)对受伤部位进行局部冷冻麻醉。请用B选择合适的方法制备氯乙烷,要求原子利用率为100%,请写出制备反应方程式
为: 
下已知A~K均为 中学化学中的常见物质,它们之间的转化关系如下图所示,其中A
中学化学中的常见物质,它们之间的转化关系如下图所示,其中A 、D为金属单质,反应过程中
、D为金属单质,反应过程中 生成的水及其他部分产物已略去。
生成的水及其他部分产物已略去。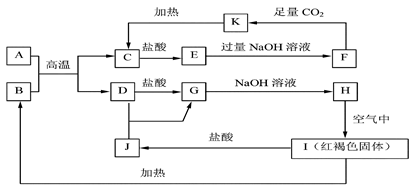
请回答以下问题:
(1)E中阳离子的结构示意图为 。
。
(2)CO2的电子式为。
(3)向F中通入足量CO2生成K的离子方程式
 。
。
(4)写出H在空气中生成I的化学方程式。
《有机化学基础》
(1)具有明显现象的官能团特征反应常被用来鉴定化合物。
①欲区分CH2 =CH2和CH3 CH3 ,应选用 __ (填字母)。
a.NaOH溶液 b.溴水 c.银氨溶液
②欲区分HCHO和HCOOH,应选用 _(填字母)。
a.KMnO4溶液 b.银氨溶液 c.Na2CO3溶液
③欲区分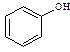 和
和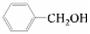 ,应选用 ___ (填字母)。
,应选用 ___ (填字母)。
a.FeCl3溶液 b.NaOH溶液 c.AgNO3溶液
(2)在有机化学中,同分异构是普遍存在现象。分子式为C4H9OH的有机物共有
种。其中,一种有机物通过消去反应可转变为2-丁烯,请写出该消去反应的化学方程式 ;另一种有机物的核磁共振氢谱图(1H核磁共振谱图)中显示一个峰,请写出该有机物的结构简式如下:。
;另一种有机物的核磁共振氢谱图(1H核磁共振谱图)中显示一个峰,请写出该有机物的结构简式如下:。
(3)A是石油裂解气的成分之一,A的某一同系物E的产量通常用来衡量一个国家的石油化工水平。现以A为主要原料合成C6H12O2,其合成路线如下图所示: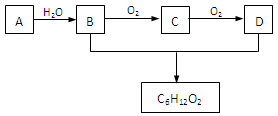
回答下列问题:
①A的结构简式为:______________。
②B、D分子中的官能团名称分别为_______________、_____________。
③写出B的同类别的同分异构体的结构简式:___________________。
④写出B→C的化学方程式:_______________________ __________________。
__________________。
《化学与生活》
(1)材料是人类赖以生存和发展的重要物质基础。
①生产水泥的主要原料是黏土和(填名称)。
②有机玻璃(聚甲基丙烯酸甲酯)实际上不是硅酸盐材料,而是一种。(选填“橡胶”或“纤维”或“塑料”)
③上海世博会中国馆用到一种涂料—氟碳涂层聚酯(FEP),它的单体为CF3—CF=CF2,这种涂料具有 (选填“热塑性”或“热固性”)。
(选填“热塑性”或“热固性”)。
④玻璃钢具有耐 腐蚀、质量轻、强度高的性能,它属于材料(选填“合金”或“复合”)。
腐蚀、质量轻、强度高的性能,它属于材料(选填“合金”或“复合”)。 (2)人体健康与食品、药物等关系密切。
(2)人体健康与食品、药物等关系密切。
①有些学生从小偏食,不爱吃水果、蔬菜,结果营养缺乏、发育不良,这主要是由于摄取______________( 选填“
选填“ 脂肪”、“维生素”或“蛋白质”)不足引起的。
脂肪”、“维生素”或“蛋白质”)不足引起的。
②生活中应合理地摄取人体必需的元素,体内________含量过高,会引起甲状腺疾病。
③糖类、油脂、蛋白质都是人体必需的营养物质。其中蛋白质被摄入人体后,在酶的作用下水解为_______________________(写名称)。
④小苏打可用来治疗胃酸过多,请写出该反应的离子方程式
________________________________________ ___________。
___________。
⑤可以帮助流感病人解热镇痛的药物是______________(选填“青霉素”或“阿司匹林”)。
( 3)洁净安全的生存环境更是健康的保障。
3)洁净安全的生存环境更是健康的保障。
①为确保上海世博会期间城市空气质 量优良率达到95%以上,世博会期间的空气质量状况监测中,不需要监测的指标是。
量优良率达到95%以上,世博会期间的空气质量状况监测中,不需要监测的指标是。
a.可吸入颗粒物(PM10) b.NO2浓度 c.SO2浓度 d.CO2浓度
②可利用漂白粉对河水进行杀菌消毒,其能杀菌消毒的原因是漂白粉会与河水反应生成HClO(用化学反应方程式表示)是 。
。
③垃圾的无害化处理常用的方法包括卫生填埋和_________________焚烧。
④人们为追求时尚而把头发染成各种各样的颜色,常见的染发剂有植物染发剂、无机染发剂和_________________染发剂(选填“ 有机”“合成”或“复合”)。
有机”“合成”或“复合”)。
在一定温度下将2 mol A和2 mol B两种气体混合于2 L密闭容器中,发生如下反应:3A(g)+B(g)  2C(g)+2D(g),2分钟末反应达到平衡状态,生成了0.8 mol D,请填写下面空白。
2C(g)+2D(g),2分钟末反应达到平衡状态,生成了0.8 mol D,请填写下面空白。
(1)用D表示的平均反应速率为_____ ____,A的转化率为______ ____。
(2)如果缩小容器容积(温度不变),则平衡体系中混合气体的密度_________(填“增大”、“减少”或“不变”)。
(3)若开始时只加C和D各4/3 mol,要使平衡时各物质的质量分数与原平衡相等,则还应加入____ mol B物质。
(4)若向原平衡体系再投入1 mol A和1 mol B,平衡__________(填“右移、左移或不移”)。
(12分)某研究性小组进行如下实验:常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
| 实验编号 |
HA物质的量浓度(mol/L) |
NaOH物质的量浓度(mol/L) |
混合溶液的pH |
| ① |
0.1 |
0.1 |
pH=9 |
| ② |
c |
0.2 |
pH=7 |
| ③ |
0.2 |
0.1 |
pH<7 |
请回答:
(1)从①组情况分析,HA是强酸还是弱酸?__________(填“强酸”或“弱酸”)。
(2)②组情况表明,c____0.2 mol/L(填﹥、﹤或=)。混合液中离子浓度c(A-)c(Na+)(填﹥、﹤或=)。
(3)从③组实验结果分析,说明HA的电离程度______NaA的水解程度 (填﹥、﹤或=),该混合溶液中离子浓度由大到小的顺序是________。
(填﹥、﹤或=),该混合溶液中离子浓度由大到小的顺序是________。
(4)①组实验所得混合溶液中由水电离出的c(OH-)=____________mol·L-1。