某氧化物难溶于水,可溶于烧碱溶液,生成易溶于水的化合物,取所得溶液,逐滴滴入过量稀盐酸,立即生成白色沉淀且逐渐增多,则原氧化物为
| A.MgO | B.Al2O3 | C.SiO2 | D.SO 2 2 |
下列气体溶于水时,发生了氧化还原反应的是
| A.Cl2溶于水 | B.NH3溶于水 | C.CO2溶于水 | D.SO2溶于水 |
环境污染问题越来越受到人们的关注,造成环境污染的主要原因大多是由于人类生产活动中过度排放有关化学物质引起的。下列环境问题与所对应的化学物质不相符的是
| A.臭氧层破坏——氟氯烃 | B.光化学烟雾——氮氧化物 |
| C.水体富营养化——含磷洗衣粉 | D.酸雨——二氧化碳 |
从实验测得不同物质中氧氧之间的键长和键能的数据:
| O—O键 数据 |
O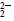 |
O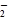 |
O2 |
O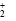 |
| 键长(10-12 m) |
149 |
128 |
121 |
112 |
| 键能(kJ·mol-1) |
x |
y |
z=494 |
w=628 |
其中x、y的键能数据尚未测定,但可根据规律性推导键能的大小顺序为w>z>y>x;该规律性是
A.成键的电子数越多,键能越大
B.键长越长,键能越小
C.成键所用的电子数越少,键能越大
D.成键时电子对越偏移,键能越大
下列说法正确的是
| A.离子化合物中可能含有共价键,但不一定含有金属元素 |
| B.分子中一定含有共价键 |
| C.非极性分子中一定存在非极性键 |
| D.极性分子中一定不存在非极性键 |
氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为
| A.两种分子的中心原子杂化轨道类型不同,NH3为sp2杂化,而CH4是sp3杂化 |
| B.NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道 |
| C.NH3分子中有一对未成键的孤电子对,它对成键电子的排斥作用较强 |
| D.氨气分子是极性分子而甲烷是非极性分子 |