食醋分为酿造醋和配制醋两种。国家标准规定酿造食醋总酸含量不得低于3.5g/100mL。
(1)某研究小组利用滴定分析法测定某品牌食醋中醋酸的含量,下列说法正确的是______
a.用NaOH溶液滴定时反应的离子方程式为:H++OH-=H2O
b.食醋试样需稀释一定倍数后再进行滴定
c.用NaOH溶液滴定食醋,可使用酚酞或甲基橙作指示剂
d.若测得该品牌食醋的物质的量浓度为0.75mol·L-1,则该食醋的总酸量为4.5g/100mL。
(2)研究小组的同学仔细观察了该品牌食醋的标签,发现其中还含有苯甲酸钠作为食品添加剂,他想用资料法验证醋酸与食品添加剂(苯甲酸钠C6H5COONa)不会发生离子互换反应,需查找在一定温度下的醋酸与苯甲酸的________ (填写序号)。
a.pH b.电离度 c.电离常数 d.溶解度
(3)常温下,用0.1000 mol·L-1NaOH溶液分别滴定20.00mL 0.1000 mol·L-1HCl溶液和20.00mL 0.1000 mol·L-1CH3COOH溶液,得到2条滴定曲线,如下图所示。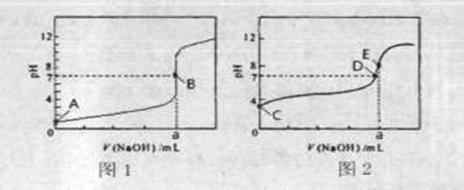
①滴定醋酸溶液的曲线是_______ (填“图l”或“图2”);滴定曲线中a=_____ mL;
②E点pH>8的原因用离子方程式表示________。
(4)现欲粗略测定一未知浓度的CH3COOH溶液的电离度,应做的实验和所需的试剂(试纸)是________(填写序号)
a.电解,NaOH溶液 b.蒸馏,Na2CO3溶液
c.酯化反应,石蕊试液 d.中和滴定,pH试纸
(5)为标定某醋酸溶液的准确浓度,用0.2000 mol?L-1 的NaOH溶液对20.00 mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
| 实验序号 |
1 |
2 |
3 |
4 |
| 消耗NaOH溶液的体积(mL) |
20.05 |
20.00 |
18.80 |
19.95 |
则该醋酸溶液的准确浓度为________ 。
某化学课外活动小组用浓盐酸、MnO2共热制Cl2,并用Cl2和Ca(OH)2反应制少量漂白粉,现已知反应2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O,正反应为放热反应,温度稍高即发生副反应6Cl2+
6Ca(OH)2=5CaCl2+Ca(ClO3)2+6H2O。甲、乙、丙三人分别设计三个实验装置,如下图所示。
(1)请指出三个装置各处的缺点或错误(如没有可不填)
甲:_______________________________________________________;
乙:_______________________________________________________;
丙:_______________________________________________________。
(2)图甲由A、B两部分组成,乙由C、D、E三部分组成,丙由F、G组成,从上述甲、乙、丙三套装置中选出合理的部分(按气流从左到右的方向)组装一套较完善的实验装置(填所选部分的编号) ___________________________________。
(3)实验中若用12mol·L-1的浓盐酸100mL与足量的MnO2反应,最终生成Ca(ClO)2的物质的量总是小于0.15mol,其可能的主要原因是(假定各步反应均无反应物损耗且无副反应发生) _______________________________________________________。
拟用如图所示装置制取表中的四种干燥、纯净的气体(图中铁架台、铁夹、加热及气体收集装置均已略去;必要时可以加热;a、b、c、d表示相应仪器中加入的试剂)。
| 气体 |
a |
b |
c |
d |
| C2H4 |
乙醇 |
浓H2SO4 |
NaOH溶液 |
浓H2SO4 |
| Cl2 |
浓盐酸 |
MnO2 |
NaOH溶液 |
浓H2SO4 |
| NH3 |
饱和NH4Cl溶液 |
消石灰 |
H2O |
固体NaOH |
| NO |
稀HNO3 |
铜屑 |
H2O |
P2O5 |
(1)上述方法中可以得到干燥、纯净的气体是____________________。
(2)指出不能用上述方法制取的气体,并说明理由。
①气体__________,理由是____________________。
②气体__________,理由是____________________。
③气体__________,理由是____________________。
( 12分 ) 为探究乙炔与溴的加成反应,甲同学设计并进行了如下实验: 先取一定量工业用电石与水反应,将生成的气体通入溴水中,发现溶液褪色,即证明乙炔与溴水发生了加成反应。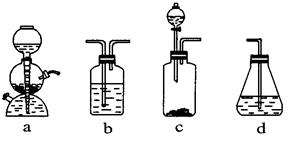
 b
b 
 b
b
(电石、水) ( ) ( ) ( 溴水 )
乙同学发现甲同学实验中,褪色后的溶液里有少许淡黄色浑浊,推测在制得的乙炔中还有可能含有少量还原性的杂质气体。由此他提出必须先除去之,再与溴水反应。
请回答问题:
( 1 ) 写出甲同学实验中两个主要的化学方程式 _______________________________ 。
( 2 ) 甲同学设计的实验 ________ ( 填“能”或“不能” ) 验证乙炔与溴发生加成反应,其理由是 __________________________________________ 。
a. 使溴水褪色的反应,未必是加成反应
b. 使溴水褪色的反应,就是加成反应
c. 使溴水褪色的物质,未必是乙炔
d. 使溴水褪色的物质,就是乙炔
( 3 ) 乙同学推测此乙炔中必定含有的一种杂质气体是 ________ ,它与溴水反应的化学方程式是 __________________________ 。验证过程中必须全部除去。
( 4 ) 请你选用上列四个装置 ( 可重复使用 ) 来实现乙同学的实验方案,将它们的编号填入方框,并写出装置内所放的化学药品。
( 5 ) 为验证这一反应是加成而不是取代,丙同学提出可用pH试纸来测试反应后溶液的酸性,理由是什么?
( 12分 ) 已知两个羧基之间在浓硫酸作用下脱去一分子水生成酸酐,如:
某酯类化合物A是广泛使用的塑料增塑剂。A在酸性条件下能够生成B、C、D。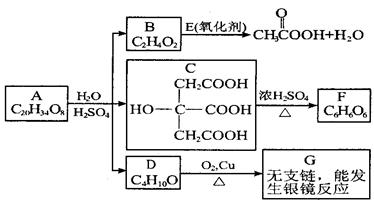
( 1 ) CH3COOOH称为过氧乙酸,写出它的一种用途 _________ 。
( 2 ) 写出 B + E  CH3COOOH + H2O 的化学方程式 ____________________ 。
CH3COOOH + H2O 的化学方程式 ____________________ 。
( 3 ) 写出F可能的结构简式 __________________ 。
( 4 ) 写出A的结构简式 ______________________ 。
( 5 ) 1 mol C分别和足量的金属Na、NaOH反应,消耗Na与NaOH物质的量之比是 _____ 。
( 6 ) 写出D跟氢溴酸 ( 用溴化钠和浓硫酸的混合物 ) 加热反应的化学方程式:
______________________________________________________ 。
( 8分 ) 有机物E和F可用作塑料增塑剂或涂料中的溶剂。它们的相对分子质量相等,可用以下方法合成: 
( 1 ) 请写出有机物的名称: A、_________ B _______________ 。
( 2 ) 请分别写出A + D E 和B + G
E 和B + G  F 的化学方程式: __________________ 。
F 的化学方程式: __________________ 。
( 3 ) X反应的类型是 _____________ ,X反应的条件是 _____________ 。
( 4 ) E与F的相互关系是 _______ ( 选填下列选项的编号 ) 。
①同系物 ②同分异构体 ③同一种物质 ④同一类物质