设NA为阿伏加德罗常数的数值,下列叙述中正确的是
| A.3.4gNH3中含有电子数为0.2NA |
| B.标准状况下,22.4 L Cl2参加所有化学反应转移的电子数一定都是2NA |
| C.标准状况下,0.5NA个SO3分子所占的体积约为11.2 L |
D.在18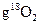 中含有 中含有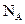 个氧原子 个氧原子 |
一定量的某饱和一元醛发生银镜反应可得21.6g银;将等量的该醛完全燃烧,生成3.6g水。此醛可能是
| A.甲醛 | B.乙醛 | C.丙醛 | D.丁醛 |
要检验溴乙烷中的溴原子,正确的实验方法是
| A.加入氯水振荡,观察水层是否有红棕色出现 |
| B.滴入AgNO3溶液,再加入稀硝酸,观察有无浅黄色沉淀生成 |
| C.加入NaOH溶液共热,然后加入稀硝酸使溶液呈酸性,再滴入AgNO3溶液,观察有无浅黄色沉淀生成 |
| D.加入NaOH溶液共热,然后加入AgNO3溶液,观察有无浅黄色沉淀生成 |
同温同压下,某有机物和过量Na反应得到V1 L氢气,取另一份等量的有机物和足量NaHCO3反应得V2 L二氧化碳,若V1=V2 ≠ 0,则该有机物可能是
A.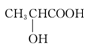 |
B.HOOC—COOH |
| C.HOCH2CH2OH | D.CH3COOH |
据最近的美国《农业研究》杂志报道,美国的科学家发现半胱氨酸能增强艾滋病毒感染者的免疫力,对控制艾滋病毒的蔓延有奇效。已知半胱氨酸的结构简式为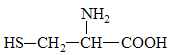 ,则下列说法错误的是
,则下列说法错误的是
A.两分子半胱氨酸脱水形成的二肽结构简式为: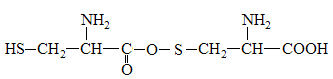 |
| B.半胱氨酸是一种两性物质 |
C.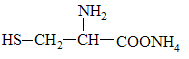 可与过量NaOH溶液反应放出氨气 可与过量NaOH溶液反应放出氨气 |
| D.天然蛋白质水解产物均为α-氨基酸 |
有机物分子中原子或原子团间的相互影响会导致化学性质的不同。下列叙述不能说明上述观点的是
| A.苯酚能与NaOH溶液反应,而乙醇不能 |
| B.丙酮(CH3COCH3)分子中的H比乙烷分子中的H更易被卤原子取代 |
| C.乙烯可发生加成反应,而乙烷不能 |
| D.苯酚能与浓溴水反应,而苯不可以 |