一定温度下,有a.盐酸;b.硫酸;c.醋酸三种酸的稀溶液。(用a、b、c、<、=、>号填写)
①当其物质的量浓度相同时,c(H+)由大到小的顺序是___________________,
②同体积同物质的量浓度的三种酸,中和NaOH能力由大到小的顺序是_____ _____,
③当其c(H+)相同时,物质的量浓度由大到小的顺序为_____________________,
④当c(H+)相同、体积相同时,分别加入足量锌,相同状况产生的气体体积由大到小的顺序为______________________。
⑤当c(H+)相同、体积相同时,同时加入形状、质量、密度相同的锌,若产生相同体积的氢气(相同状况),则开始时反应速率的大小关系是__________________,反应所需的时间的长短关系是__________________。
⑥将c(H+)相同的三种酸均加水稀释至原来的10倍,c(H+)由大到小的顺序为___ __________。
在标准状况下,空气中N2和O2的体积比约为4∶1,则N2和O2的物质的量之比为_________,空气的密度约为_________,空气的平均相对分子质量为_________。
在过氧化钠与水的反应中,若有0.1 mol的过氧化钠参加反应,则有:
(1)转移的电子总数为。
(2)参加反应的氧化剂的物质的量为mol。
(3)有个氧气分子生成。
(4)参加反应的还原剂的物质的量为mol。
将红磷与氯气按1∶1.8的物质的量比混合,点燃使其充分燃烧,发生如下反应:2P+3Cl2 2PCl3、PCl3+Cl2
2PCl3、PCl3+Cl2 PCl5,完全反应后氯气没有剩余,则生成物中三氯化磷与五氯化磷的物质的量之比为。
PCl5,完全反应后氯气没有剩余,则生成物中三氯化磷与五氯化磷的物质的量之比为。
(1)标准状况下,用氨气做喷泉实验,实验完毕后,液体进入烧瓶总容积的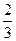 。假设溶质不外泄,则所得溶液的物质的量浓度为_________________________。
。假设溶质不外泄,则所得溶液的物质的量浓度为_________________________。
(2)标准状况下,1体积水可以溶解700体积氨气,所得溶液的密度为0.90 g·mL-1,则所得氨水的物质的量浓度为__________________。
在1.00 L 1.00 mol·L-1 NaOH溶液中通入16.8 L标准状况下的CO2,计算所得溶液中含有NaHCO3和Na2CO3的物质的量。