在标准状况下①6.72L CH4 ②3.01×1023个HCl分子 ③ 13.6g H2S ④0.2mol NH3,下列对这四种气体的关系从大到小表达正确的是:
13.6g H2S ④0.2mol NH3,下列对这四种气体的关系从大到小表达正确的是:
a.体积 ②>③>①>④ b.密度 ②>③>④>①
c.质量 ②>③>①>④ d.氢原子个数 ①>③>④>②
| A.abc | B.bcd | C.abcd | D.acd |
 和
和 是氧元素的两种同位素,
是氧元素的两种同位素, 表示阿伏伽德罗常数,下列说法正确的是()
表示阿伏伽德罗常数,下列说法正确的是()
A. 与 与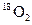 互为同分异构体 互为同分异构体 |
B. 与 与 核外电子排布方式不同 核外电子排布方式不同 |
C.通过化学变化可以实现 与 与 间的相互转化 间的相互转化 |
D.标准状况下,1.12L 和1.12L 和1.12L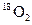 均含有0.1 均含有0.1 个氧原子 个氧原子 |
下列排列顺序不正确的是()
| A.粒子半径:Al3+ < Mg2+ < F- |
B.热稳定性:HI > HBr > HCl > HF HCl > HF |
| C.酸性: H2SiO3< H3PO4< H2SO4< HClO4 |
| D.碱性: NaOH > Mg(OH)2> Al(OH)3 |
下列说法中,正确的是()
A.离子化合物中一定不含共价键,共价化合物中一定不含离 子键 子键 |
| B.水分子呈直线形,氨分子呈三角锥形 |
| C.碳原子之间可形成碳碳单键、碳碳双键或碳碳叁键 |
| D.分子间作用力越大,分子的热稳定性就越大 |
可逆反应H2(g)+I2(g) 2HI(g)达到平衡状态时的标志是( )
2HI(g)达到平衡状态时的标志是( )
| A.混合气体的体积恒定不变 | B.混合气体的颜色不再改变 |
| C.H2、I2、HI的浓度相等 | D.I2在混合气体中的体积分数与H2在混合气体中的体积分数相等 |
要制取纯净气体,必须根据气体的逸出环境分析可能含有的杂质,再根据气体本身和杂质的性质决定除杂方案。干燥是除去水蒸气的一种除杂方法,下列不能用来干燥氯气的干燥剂是( )
| A.浓硫酸 | B.五氧化二磷 | C.无水氯化钙 | D.生石灰 |