某恒温密闭容器发生可逆反应Z(?)+W(?) X(g)+Y(?) ΔH ,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件。下列有关说法中不正确的是
X(g)+Y(?) ΔH ,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件。下列有关说法中不正确的是 
| A.Z和W在该条件下一定不为气态 |
| B.t1~t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量不可能相等 |
| C.若在该温度下此反应平衡常数表达式为K=c(X),则t1~t2时间段与t3时刻后的X 浓度相等 |
| D.若该反应只在某温度T0以上自发进行,则该反应的平衡常数K随温度升高而增大 |
固体氧化物燃料电池(SOFC)以固体氧化物作为电解质。其工作原理如右图所示:下列关于固体燃料电池的有关说法正确的是
A.电极b为电池负极,电极反应式为O2+4e-=4O2-
B.固体氧化物的作用是让电子在电池内通过
C.若H2作为燃料气,则接触面上发生的反应为
H2+2OH--4e-=2H++H2O
D.若C2H4作为燃料气,则接触面上发生的反应为
C2H4+6O2--12e-=2CO2+2H2O
500mL KNO3和Cu(NO3)2的混合溶液中c(NO3-)=6.0 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4 L气体(标准状况),假定电解后溶液体积仍为500 mL,下列说法正确的是
| A.原混合溶液中c(K+)为2 mol·L-1 | B.上述电解过程中共转移2 mol电子 |
| C.电解得到的Cu的物质的量为0.5 mol | D.电解后溶液中c(H+)为2 mol·L-1 |
观察下列几个装置示意图,有关叙述正确的是()
| A.装置①中阳极上析出红色固体 |
| B.装置②的待镀铁制品应与电源正极相连 |
| C.装置③闭合电键后,外电路电子由a极流向b极 |
| D.装置④的离子交换膜允许阳离子、阴离子、水分子自由通过 |
关于右图所示的原电池,下列说法正确的是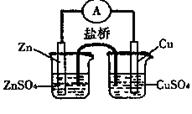
| A.电子从铜电极通过检流计流向锌电极 |
| B.盐桥中的阳离子向硫酸铜溶液中迁移 |
| C.锌电极发生还原反应,铜电极发生氧化反应 |
D.铜电极上发生的电极反应是 |
下列事实于氢键有关的是
| A.水加热到很高的温度都难以分解 | B.水结成冰体积膨胀,密度变小 |
| C.CH4、SiH4、GeH4、SnH4熔点随着相对分子质量的增大而升高 | |
| D.HF、HCl、HBr、HI的热稳定性依次减弱 |