高温下,某反应达平衡,平衡常数K=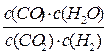 。恒容时,温度升高,H2浓度减小。下列说法正确的是( )
。恒容时,温度升高,H2浓度减小。下列说法正确的是( )
A.该反应的焓变为正值 |
B.恒温恒容下,充入CO ,[H2]会减小 |
| C.升高温度,逆反应速率减小 | D.该反应化学方程式为CO+H2O CO2+H2 CO2+H2 |
pH与体积都相同的硫酸和醋酸溶液,分别与同物质的量浓度、同体积的Na2CO3溶液反应,若在相同条件下放出CO2的量相同,则下列推断合理的是
| A.Na2CO3过量 | B.Na2CO3恰好与醋酸完全反应 |
| C.Na2CO3恰好与硫酸完全反应 | D.两种酸都过量 |
将0.2mol/L的醋酸钠溶液10mL与0.1mol/L盐酸10mL混合后,溶液显酸性,则溶液中有关微粒的浓度关系正确的是
| A.c(Na+)+c(H+)=c(Ac-)+c(Cl-)+c(OH-) | B.c(HAc)>c(Cl-)>c(Ac-)>c(H+) |
| C.c(Ac-)>c(Cl-)>c(HAc)>c(H+) | D.c(Ac-)=c(Cl-)=c(HAc)>c(H+) |
利用下列装置(部分仪器已省略),能顺利完成对应实验的是
| A.制硝基苯 | B.制氢氧化亚铁 | C.实验室制乙烯 | D.石油的蒸馏 |
下列离子方程式,一定正确的是
| A.硫化亚铁与稀硝酸反应:FeS+2H+→Fe2++H2S |
| B.纯碱溶液中滴加少量盐酸:CO32- + H+ → HCO3- |
| C.过量的NaHSO4与Ba(OH)2溶液反应:Ba2++2OH-+2H++SO42-→BaSO4↓+2H2O |
| D.将少量SO2气体通入Ca(ClO)2溶液中:SO2+Ca2++2ClO-+H2O→CaSO3↓+2HClO |
在铁与铜的混和物中,加入一定量的稀硝酸,充分反应后剩余金属m1g,再向其中加入一定量的稀硫酸,充分振荡后,剩余金属m2g,m1与m2的关系是
| A.m1 g固体中一定有铁 | B.m1一定大于m2 |
| C.m1可能等于m2 | D.m1可能大于m2 |