可逆反应mA(s)+nB(g)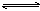 pC(g)+qD(g)反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图(T2>T1),根据图中曲线分析,判断下列叙述中正确的是
pC(g)+qD(g)反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图(T2>T1),根据图中曲线分析,判断下列叙述中正确的是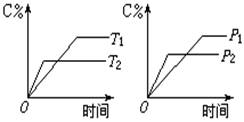
| A.到达平衡后,若使用催化剂,C的质量分数增大 |
| B.平衡后,若升高温度,平衡则向逆反应方向移动 |
| C.平衡后,增大A的量,有利于平衡向正反应方向移动 |
| D.化学方程式中一定n>p+q |
课堂学习中,同学们利用铝条、锌片、铜片、导线、电流计、橙汁、烧杯等用品探究原电池的组成。下列结论错误的是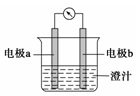
| A.原电池是将化学能转化成电能的装置 |
| B.原电池由电极、电解质溶液和导线等组成 |
| C.图中a极为铝条、b极为锌片时,导线中会产生电流 |
| D.图中a极为锌片、b极为铜片时,电子由铜片通过导线流向锌片 |
CuSO4溶液中加入过量KI溶液,产生白色CuI沉淀,溶液变棕色。向反应后溶液中通入过量SO2,溶液变成无色。下列说法不正确的是
| A.滴加KI溶液时,KI被氧化,CuI是还原产物 |
| B.通入SO2后,溶液变无色,体现SO2的还原性 |
| C.整个过程发生了复分解反应和氧化还原反应 |
| D.上述实验条件下,物质的氧化性:Cu2+>I2>SO2 |
铅蓄电池在现代生活中有广泛应用,其电极材料是Pb 和PbO2,电解液是H2SO4溶液。现用铅蓄电池电解饱和硫酸钠溶液一段时间,假设电解时温度不变且用惰性电极,下列说法不正确的是
| A.蓄电池放电时,电路中每转移2 mol电子,最多有1 molPbO2被还原 |
| B.电解池的阳极反应式为:4OH--4e-=2H2O+O2↑ |
| C.电解后,c(Na2SO4)不变,且溶液中有晶体析出 |
| D.蓄电池中每生成1mol H2O,电解池中就消耗1mol H2O |
下列说法正确的是
| A.利用高纯度二氧化硅制造的太阳能电池板可将光能直接转化为电能 |
| B.硝化甘油、火棉、TNT均是硝酸酯化反应以后的产物 |
| C.煤中加入生石灰、汽车中加装尾气处理装置、利用二氧化碳制造全降解塑料都能有效减少环境污染 |
| D.红外光谱法、紫外光谱法、核磁共振、同位素示踪法等都是现代化学测定有机物结构的常用方法 |
从下列实验事实所得出的结论,正确的是
| 实验事实 |
结论 |
|
| ① |
Cl2的水溶液可以导电 |
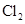 是电解质 是电解质 |
| ② |
常温下,0.1mol/LNaA与NaB溶液的pH前者大 |
酸性:HA<HB |
| ③ |
常温下,白磷可自燃而硫不与氧气反应 |
非金属性:P>S |
| ④ |
某溶液中滴加KSCN溶液,溶液变为血红色 |
该溶液含有Fe3+ |
A.③④ B.②④ C.①② D.全部