甲乙两人分别用不同的方法配制100ml 3.6mol/L的稀硫酸。
(1)甲:量取20 mL18 mol/L浓硫酸,小心地倒入盛有少量水的烧杯中,搅拌均匀,待冷却至室温后转移到100 mL容量瓶中,用少量的水将烧杯等仪器洗涤2~3次,每次洗涤液也转移到容量瓶中,然后小心地向容量瓶加入水至刻度线定容,塞好瓶塞,反复上下颠倒摇匀。
①实验所用的玻璃仪器除烧杯和容量瓶外,还有 ;
②将溶液转移到容量瓶中的正确操作是 ;
③定容的正确操作是
(2)乙:用100 mL量筒量取20 mL18 mol/L浓硫酸,并向其中小心地加入少量水,搅拌均匀,待冷却至室温后,再加入水至100 mL刻度线,再搅拌均匀。你认为此法是否正确?若不正确,指出其中错误之处 。
某光卤石(KCl·MgCl2·6H2O)样品中含有不跟NaOH溶液和盐酸反应的杂质,某校化学课外活动研究小组现欲测定此样品中含KCl·MgCl2·6H2O的质量分数,经讨论有多种实验测定方案。
请根据提供的实验试剂和仪器(所需的仪器任选),选择精确度较高的实验测定方案,简要写出第二步以后的实验步骤和实验结果。
一、可选用的实验试剂:
(1)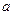 mol·L
mol·L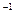 NaOH溶液 (2)
NaOH溶液 (2)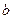 mol·L
mol·L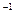 Na2CO3溶液 (3)c mol·L
Na2CO3溶液 (3)c mol·L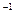 HCl溶液
HCl溶液
(4)d mol·L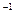 AgNO3溶液 (5)酚酞试液 (6)甲基橙试液
AgNO3溶液 (5)酚酞试液 (6)甲基橙试液
二、实验步骤:
第一步:称取m g样品,放入250mL烧杯中,加适量水溶解
第二步:
计算样品中含KCl·MgCl2·6H2O(相对分子质量为277.5)的质量分数的表达式:
。
浓氨水可与新制生石灰作用生成氨气,干燥的氨气在高温下能被CuO氧化成N2实验室欲用图仪器装置和药品来制取纯净的氮气。
试回答下列问题:
(1)这些装置按气流方向自左向右的连接顺序是(填A、B、C……)________。
(2)E中发生反应的化学方程式是________。
(3)装置④中应当选用的干燥剂是(写名称)___________。
(4)装置①中发生氧化还原反应的化学方程式是___________。其中氧化剂是______,氧化产物是________(写化学式)。
(5)装置②中浓硫酸的作用是_________。
由几种离子化合物组成的混合物,含有以下离子中的若干种:K+、NH4+、Mg2+、Ba2+、C1—、SO42—、CO32-。将该混合物溶于水后得澄清溶液,现取3份100mL该溶液分别进行如下实验:
| 实验序号 |
实验内容 |
实验结果 |
| 1 |
加AgNO3溶液 |
有白色沉淀生成 |
| 2 |
加足量NaOH溶液并加热 |
收集到气体1.12L(已折算成标准 状况下的体积) |
| 3 |
加足量BaC12溶液时,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量稀盐酸,然后干燥、称量 |
第一次称量读数为6. 27g,第二次 称量读数为2.33g |
试回答下列问题:
(1)根据实验1对C1—是否存在的判断是 (填“一定存在”、“一定不存在”或“不能确定”);根据实验1~3判断混合物中一定不存在的离子是 。
(2)试确定溶液中一定存在的阴离子及其物质的量浓度(可不填满):
| 阴离子符号 |
物质的量浓度(mol·L—1) |
(3)试确定K+是否存在? ,判断的理由是
下列装置或操作能达到实验目的的是()
某兴趣小组同学共同设计了如图所示的实验装置,既可用于制取气体,又可用于验证物质的性质。请回答下列问题:
(1)利用装置I制取某些气体,制取气体的反应所具有的特点是___________________。
(2)利用装置Ⅰ、II制取气体(K2关闭,K1打开)。甲同学认为:利用装置Ⅱ可以收集H2、NH3等气体,但不能收集O2和NO,理由是
。
乙同学认为:利用装置II作简易改进(不改变仪器装置),可收集NO、O2,改进的方法是__________________ 。
丙学认为:利用装置II作简易改进(改变仪器装置),可收集NO2气体,改进的方法是_______________________ 。
(3)利用装置I、Ⅲ 验证物质的性质(K2打开,K1关闭)。如设计实验证明氧化性:KMnO4>Cl2>Br2,则在A中加浓盐酸,B中加________ __,C中加______________ ,观察到C中的现象是___________________ 。