下列化学方程式不能用离子方程式2H++CO32-=H2O+CO2↑表示的是
A.2HCl + Na2CO3 =" 2NaCl" + H 2O+ CO2↑ 2O+ CO2↑ |
| B.2HNO3 + BaCO3 = Ba(NO3)2 + H2O + CO2↑ |
| C.H2SO4 + Na2CO3 = Na2SO4 + H2O + CO2↑ |
| D.H2SO4 +(NH4)2CO3 = (NH4)2SO4 + H2O + CO2↑ |
下列说法正确的是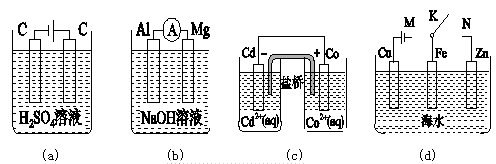
| A.图(a)中,随着电解的进行,溶液中H+的浓度越来越小 |
| B.图(b)中,Mg电极作电池的负极 |
| C.图(c)中,发生的反应为Co+Cd2+=Cd+Co2+ |
| D.图(d)中,K分别与M、N连接时,Fe电极均受到保护 |
将足量的CO2不断通入KOH、Ba(OH)2、KA1O2的混合溶液中,生成沉淀与通入CO2的量的关系可表示为
下列物质间的转化在给定条件下能实现的是
| A.②④ | B.③④ | C.①④ | D.①②③ |
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.0.1mol苯中含有双键的数目为0.3NA |
| B.7.8g 由Na2S和Na2O2组成的混合物中含有阴离子的数目为 0.1NA |
| C.标准状况下,22.4 L乙醇中含有分子的数目为NA |
| D.在过氧化钠与水的反应中,每生成0.1mol 氧气,转移电子的数目为0.4NA |
下列选项中,离子方程式书写正确的是
| A.向硝酸银溶液中加入足量的氨水:Ag+ +2NH3·H2O = Ag(NH3)2+ + 2H2O |
| B.向Fe(NO3)2和KI混合溶液中加入少量稀盐酸:3Fe2++4H++NO3-= 3Fe3++ 2H2O+NO↑ |
| C.泡沫灭火器的灭火原理:2Al3+ +3CO32-+3H2O = 2Al(OH)3↓+ 3CO2↑ |
| D.用足量的氨水处理合成氨工业的尾气:SO2+ NH3·H2O = NH4+ + HSO3- |