下列说法正确的是( )
A.某溶液中所有离子的浓度大小排序是:c(CH3COO—)>c(Na+)>c(H+)>c(OH—),则该溶液的溶质一定是CH3COONa和C H3COOH
H3COOH
B .CH3COOH与NaOH的混合溶液显碱性,则溶液中各离子浓度大小排序一定为
.CH3COOH与NaOH的混合溶液显碱性,则溶液中各离子浓度大小排序一定为
c(Na+)>c(CH3COO—)>c(OH—)>c (H+)
C.常温下,a mol/L 的CH3COOH溶液与b mol/L NaOH溶液等体积混合后溶液的pH=7,则一定有a=b
D.常温下,pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合后溶液的pH一定等于7
已知下列数据:
2Fe(s)+O2(g)===2FeO(s)ΔH=-544 kJ·mol-1
4Al(s)+3O2(g)===2Al2O3(s)ΔH=-3 350 kJ·mol-1
则2Al(s)+3FeO(s)===Al2O3(s)+3Fe(s)的ΔH是
| A.-859 kJ·mol-1 | B.+859 kJ·mol-1 |
| C.-1 403 kJ·mol-1 | D.-2 491 kJ·mol-1 |
25 ℃、101 kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5 kJ·mol-1、285.8 kJ·mol-1、890.3 kJ·mol-1、2 800 kJ·mol-1,则下列热化学方程式正确的是
A.C(s)+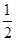 O2(g)===CO(g)ΔH=-393.5 kJ·mol-1 O2(g)===CO(g)ΔH=-393.5 kJ·mol-1 |
| B.2H2(g)+O2(g)===2H2O(g)ΔH=+571.6 kJ·mol-1 |
| C.CH4(g)+2O2(g)===CO2(g)+2H2O(g)ΔH=-890.3 kJ·mol-1 |
D.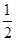 C6H12O6(s)+3O2(g)===3CO2(g)+3H2O(l)ΔH=-1 400 kJ·mol-1 C6H12O6(s)+3O2(g)===3CO2(g)+3H2O(l)ΔH=-1 400 kJ·mol-1 |
已知2H2(g)+O2 (g)===2H2O(g) ΔH=-483.6 kJ/mol。下列说法或表达正确的是
| A.在相同的条件下,2 mol氢气与1 mol氧气的总能量小于2 mol水蒸气的总能量 |
B.H2(g)+ O2(g)===H2O(l) ΔH=-Q1 kJ/mol 则Q1>241.8 O2(g)===H2O(l) ΔH=-Q1 kJ/mol 则Q1>241.8 |
C.H2(g)+ O2(g)===H2O(l) ΔH=-Q2 kJ/mol 则Q2<241.8 O2(g)===H2O(l) ΔH=-Q2 kJ/mol 则Q2<241.8 |
| D.任何条件下,2 L水蒸气分解成2 L氢气与1 L氧气需吸收483.6 kJ热量 |
一种“即食即热型快餐”适合外出旅行时使用。其内层是用铝箔包裹的、并已加工好的真空包装食品,外层则是分别包装的两包化学物质,使用时拉动预留在外的拉线,使这两种化学物质反应,此时便可对食物进行加热,这两包化学物质最合适的选择是
| A.浓硫酸与水 | B.熟石灰与水 |
| C.生石灰与水 | D.氯化钠与水 |
下列说法正确的是
| A.热化学方程式中,如果没有注明温度和压强,则表示反应热是在标准状况下测得的 |
| B.升高温度或加入催化剂,可以改变化学反应的反应热 |
| C.据能量守恒定律,反应物的总能量一定等于生成物的总能量 |
| D.物质发生化学变化一定伴随着能量变化[ |