有镁铝混合物粉末10.2g,将它溶于500ml 4 mol/L的盐酸里,若要使沉淀的质量达到最大值,则需要加入2 mol/L的氢氧化钠的体积为
| A.1000 ml | B.500 ml | C.100 ml | D.1500 ml |
下列说法正确的是
| A.不用其他试剂无法鉴别下列四种溶液:Na2CO3、Al2(SO4)3、NaCl、NaHSO4, |
| B.可以用分液漏斗分离下列三组液态混合物:硝基苯和水、油酸和水、乙酸乙酯和乙醇 |
| C.实验室保存少量液溴和白磷常用水封 |
| D.浓碱溶液沾到了皮肤上要立即用盐酸冲洗 |
为实现“绿色奥运”,下列环保建议中你认为可以采纳的是
①用天然气代替汽油和柴油作为发动机燃料
②开发生产无汞电池
③提倡使用一次性发泡塑料餐具和塑料袋
④分类回收垃圾
⑤开发利用无磷洗涤剂
| A.①③④ | B.②③④⑤ | C.①②④⑤ | D.全部 |
将2 mol A和1 mol B充入某密闭容器中发生反应:2A(g)+B(g) xC(g),达到化学平衡后,C的体积分数为
xC(g),达到化学平衡后,C的体积分数为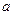 。假设该反应的条件分别和下列各选项的条件相同,下列判断正确的是
。假设该反应的条件分别和下列各选项的条件相同,下列判断正确的是
A.若在恒温恒压下,当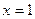 时,按1.5 mol A、l mol C作为起始物质,达到平衡后, C的体积分数仍为
时,按1.5 mol A、l mol C作为起始物质,达到平衡后, C的体积分数仍为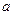
B.若在恒温恒容下,当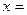 2时,将2mol C作起始物质,达到平衡后,C的体积分数仍为
2时,将2mol C作起始物质,达到平衡后,C的体积分数仍为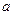
C.若在恒温恒压下,当 时,l mol A、1mol B、6mol C作起始物质,达到平衡后,C的体积分数仍为
时,l mol A、1mol B、6mol C作起始物质,达到平衡后,C的体积分数仍为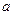
D.若在恒温恒容下,按0.6mol A、0.3mol B、1.4mol C作起始物质,达到平衡后,C的体积分数仍为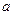 ,则
,则 为2或3
为2或3
据联合国世界卫生组织调查,当今缺铁性贫血是世界上最流行的营养性问题。我国缺铁性贫血发生率达到15%至20%,为此2004年10月9日卫生部启动和推广铁强化酱油计划,以预防缺铁性贫血。所谓铁强化酱油即在普通酱油中加入无铁腥味、极易被人体吸收的添加剂——EDTAFeNa(化学名:乙二胺四乙酸铁钠,通常带三个结晶水,分子式为:C10H12FeN2NaO8·3H2O),其中EDTAFe是一种络合铁,EDTAFe—Na的结构式为: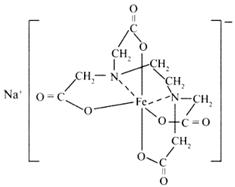
EDTA的结构简式为:(HOOCCH2)2NCH2CH2N(CH2COOH)2,下列说法正确的是
| A.EDTAFeNa中铁为+2价 | B.EDTAFeNa中铁为+3价 |
| C.EDTA属于有机物 | D.人体血液中血红蛋白中铁为+3价 |
X、Y两种元素均为短周期元素,X元素的原子所具有的电子层数为其最外层电子数的二分之一。下列有关判断中,正确的是
| A.X元素在周期表中的位置只能是第二周期第ⅣA族 |
B.若X的常见简单阴离子X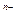 能跟Y的单质发生氧化还原反应,则说明Y的非金属性比X的强 能跟Y的单质发生氧化还原反应,则说明Y的非金属性比X的强 |
| C.若Y的非金属性比X的强,则与同一种还原剂反应时,一个Y原子得到的电子数一定比一个X原子得到的电子数少 |
D.若X能形成XO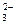 、XO 、XO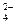 和X2O 和X2O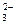 ,Y能形成YO ,Y能形成YO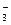 和XO 和XO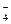 ,则X、Y一定在同一周期 ,则X、Y一定在同一周期 |