如下图所示装置中,b电极用金属M制成,a、c、d为石墨电极,接通电源,金属M沉积于b极,同时a、d电极上产生气泡。
试回答:
(1)a为 极,c极的电极反应式为: 。
(2)电解开始时,在B烧杯的中央滴几滴淀粉溶液,你能观察到的现象是

 。电解进行一段时
。电解进行一段时
间后,罩在c极上的试管中 也收集到了气体,此时c极上的电极反应式为: 。
也收集到了气体,此时c极上的电极反应式为: 。
(3)当d电极上收集到44.8 ml气体(标准状况)时停止电解,a极上放出了 mol气体,若b电极上沉积金属M的质量为0.432g,则此金属的摩尔质量为 。若要使A池中溶液恢复原浓度,应加 。
(4)电解停止后加蒸馏水使A烧杯中的溶液体积仍为200 ml,取这种溶液加入到25.0 ml 0.100 mol·L-1的HCl溶液中,当加入31.25 ml 溶液时刚好沉淀完全。由此可知电解前A烧杯中MNO3 溶液的物质的量浓度为 mol·L-1。
溶液的物质的量浓度为 mol·L-1。
(10分)在实验室里,某同学取一小块金属钠做与水反应的实验。试完成下列问题:
(1)切开的金属钠暴露在空气中,最先观察到的现象是,所发生反应的化学方程式是。
(2)将钠投入水中后,钠融化成一个小球,根据这一现象你能得出的结论是
①,②。
将一小块钠投入盛有饱和石灰水的烧杯中,不可能观察到的现象是
| A.有气体生成 | B.钠融化成小球并在液面上游动 |
| C.溶液底部有银白色的金属钙生成 | D.溶液变浑浊 |
(3)钠与水反应的离子方程式为。
在反应过程中,若生成标准状况下224mL的H2,则转移的电子的物质的量为。
(4)根据上述实验过程中钠所发生的有关变化,试说明将金属钠保存在煤油中的目的是
。
肉桂醛在食品、医药化工等方面都有重要应用。
(1)下列是合成肉桂醛、制备肉桂酸的反应路线: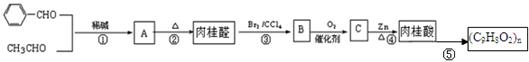

实验表明:
Ⅰ. A既能发生银镜反应,又能与金属钠反应放出氢气;
Ⅱ. 肉桂醛的相对分子质量不超过140,其中碳氢元素质量分数为87.89%。
Ⅲ. 核磁共振氢谱表明肉桂醛分子中有六种氢,其峰面积之比为1:1:1:2:2:1;
(1)A中含有的官能团为
(2) 请写出肉桂醛的结构简式。
————————————————————————————
(3) 已知反应①的原子利用率为100%,请写出第①步的化学反应方程式。
(4)反应(1)的反应类型反应(2)的反应类型为
(5) 请写出上述合成路线中使用③④两步反应的目的。
(6)写出反应⑤的化学方程式。
(7) 请写出与肉桂醛互为同分异构体,且同时满足 a.分子中无甲基,b.所有碳原子一定在同一平面上c、苯环上一氯代物只有两种的有机物的结构简式。
新制氯水中含有多种粒子,某校化学研究性学习小组的同学为探究其性质,做了如下实验,请你帮助完成:
(1)氯气能使湿润的红色布条褪色。使其褪色的微粒的化学式是______
(2)将氯水在光照上一段时间,溶液颜色逐渐变浅,其有关反应的化学方程式为:
、
(3)平衡常数表明了封闭体系的可逆反应在给定的温度下进行的程度,对于同一个类型的反应,平衡常数越大,表明反应进行的程度 越大。
越大。
H2CO3
 + H+ Ka1(H2CO3)=4.45×10—7
+ H+ Ka1(H2CO3)=4.45×10—7

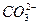 +H+ Ka2(HCO3-)=5.61×10-11
+H+ Ka2(HCO3-)=5.61×10-11
HclO  H++
H++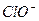 Ka(HClO)=2.95×10-8
Ka(HClO)=2.95×10-8
请依据以上电离平衡常数,请写出将少量的氯气通入到过量的碳酸钠溶液中所发生反应的离子方程式:
(4)饱和氯水与石灰石的反应是制取较浓HClO溶液的方法之一。
实验一、定性研究:
①在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,
有少量气泡产生,溶液浅黄绿色褪去;
② 过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强;
③ 为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体;
将第三份加热,看到溶液变浑浊且有大量无色气体产生。
经检测,上述实验中产生的无色气体均为CO2。
请回答:
① 反应后所得的溶液漂白性增强的原因是_____________________
②依据上述实验可推知:②的滤液中的溶质除CaCl2、HClO外,还含有_______。
实验二、定量研究:
在圆底烧瓶底部,有一用塑料网包住的过量块状碳酸钙和150mL饱和氯水,按如图所示装置实验,待不再产生气泡后,将塑料网中剩余的石灰石提出液 面,密封后再加热、煮沸烧瓶中的液体,直到量筒中的气体不再增加(不考虑HClO的分解)。
面,密封后再加热、煮沸烧瓶中的液体,直到量筒中的气体不再增加(不考虑HClO的分解)。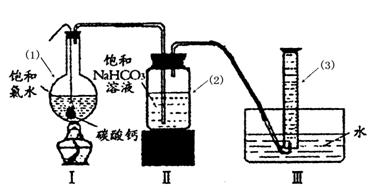
请回答:
③写出仪器(1)与仪器(3)的名称
(1)(3)
④为减少用装置Ⅲ收集气体过程中CO2因溶解而造成的损失,且水槽中仍然为水,请你对装置Ⅲ进行改进,最简单的方法是。
⑤如何准确读出量筒中气体的体积
a_________
b 上下移动量筒至量筒内液面与水槽液面相平
c
浓硫酸与木炭粉在加热条件下反应:C+2H2SO4(浓) CO2↑+2H2O+2SO2↑
CO2↑+2H2O+2SO2↑
Ⅰ、第一小组用下图所示各装置设计一个实验,验证上述反应所产生的三种产物。 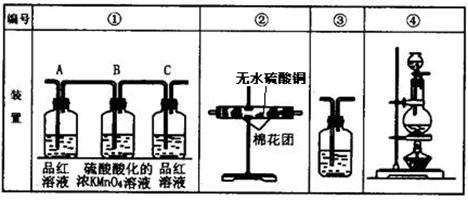
(1)这些装置的连 接顺序(按产物气流从左到右的方向)是(填装置的编号):
接顺序(按产物气流从左到右的方向)是(填装置的编号): ④ →__________→__________→__________。
④ →__________→__________→__________。
(2)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色。A瓶溶液变化体现了SO2 性,B瓶溶液反应是利用SO2 性。
B瓶溶液的作用是 ,
C瓶溶液的作用是 。
(3)实验时装置②中看到现象是 。
(4)装置③中所加的试剂名称是 ,现象是 。
Ⅱ、另一小组为测得CO2和SO2的质量,并算两者物质的量比,设计下列实验:
将生成气体依次通过X溶液→浓硫酸→碱石灰1→碱石灰2,并设法让气体完全被吸收。
(1)下列试剂中可以充当X的是: ( )
| A.BaCl2溶液 | B.Ba(OH)2溶液 |
| C.滴加H2O2的BaCl2溶液 | D.滴加H2O2的Ba(OH)2溶液 |
(2)实验结束后,在X溶液中得到的沉淀通过过滤、洗涤、烘干、称重,称得质量为ag。称得碱石灰1在实验前后 增重质量为bg。用a、b表示CO2和SO2的物质的量比 。
增重质量为bg。用a、b表示CO2和SO2的物质的量比 。
某合作小组同学将铜片加入稀硝酸,发现开始时反应非常慢,一段时间后反应速率明显加快。该小组通过实验探究其原因。该反应的离子方程式为________________________________________________。
提出合理假设。该实验中反应速率明显加快的原因可能是__________。
| A.反应放热导致温度升高 | B.压强增大 |
| C.生成物的催化作用 | D.反应物接触面积增大 |
初步探究。测定反应过程中溶液不同时间的温度,结果如下表:
| 时间/min |
0 |
5 |
10 |
15 |
20 |
25 |
35 |
50 |
60 |
70 |
80 |
| 温度/℃ |
25 |
26 |
26 |
26 |
26 |
26 |
26.5 |
27 |
27 |
27 |
27 |
结合实验目的和表中数据,你得出的结论是__________________________________。进一步探究。查阅文献了解到化学反应的产物(含中间产物)可能对反应有催化作用,请完成以下实验设计表并将实验目的补充完整:
| 实验编号 |
铜片质量/g |
0.1mol·L-1的硝酸体积/mL |
硝酸铜晶体/g |
亚硝酸钠晶体/g |
实验目的 |
| ① |
5 |
20 |
实验①和②探究_________的影响;实验①和③探究亚硝酸根的影响。 |
||
| ② |
0.5 |