一定条件下,在一恒容密闭容器中进行反应:2SO2(g)+O2(g)  2SO3(g) ,下列表述不能判断其是否达到化学平衡状态的是
2SO3(g) ,下列表述不能判断其是否达到化学平衡状态的是
| A.容器中的压强不再发生变化 |
| B.SO2、O2、SO3的浓度不再发生变化 |
| C.容器中气体的密度不再发生变化 |
| D.单位时间内生成nmol O2同时消耗2nmol SO2 |
设NA代表阿佛加德罗常数,下列说法不正确的是
| A.1.5molNO2与足量的H2O反应,转移的电子数为NA |
| B.常温常压下,0.5NA个CO2分子质量为22g |
| C.28克氮气所含的原子数目为NA |
| D.在标准状况下,0.5NA个氯气分子所占体积是11.2L |
下列涉及离子方程式书写的评价合理的是
| 选项 |
化学反应及离子方程式 |
评价 |
| A |
醋酸钠溶于水:CH3COO-+H2O=CH3COOH+OH- |
正确 |
| B |
实验室用浓盐酸与MnO2反应制Cl2: |
错误,反应物中HCl电离出的H+、Cl-比例为1:1 |
| C |
硝酸铁溶液中加过量氨水:Fe3++3NH3·H2O= Fe(OH)3(胶体)+3NH4+ |
错误,Fe(OH)3应该是沉淀 |
| D |
NH4HCO3溶液与过量的NaOH溶液反应: HCO3-+OH-=CO32-+H2O |
正确 |
下列说法正确的是
| A.用浓溴水可以鉴别苯、甲苯、环己烷 |
| B.所有的蛋白质、塑料、橡胶均难溶于水 |
| C.糖类化合物由碳、氢、氧三种元素组成[ |
| D.乙烯、乙醛、乙醇、乙酸、乙烷均可以使酸性高锰酸钾溶液褪色 |
将4 mol A和2 mol B在2L的密闭容器中混合并在一定的条件下发生如下反应:
2A(g)+ B(g)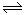 2C(g),经2秒后测得C的浓度为0.6 mol•L-1,现有以
2C(g),经2秒后测得C的浓度为0.6 mol•L-1,现有以
下几种说法:
①用物质A表示的该反应的平均反应速率为0.3 mol•L-1• s -1
②用物质B表示的该反应的平均反应速率为0.6 mol•L-1• s -1
③2s时物质B的物质的量的浓度为0.7 mol•L-1
④2s时物质A的转化率为70%
其中表述正确的是()
下列说法正确的是()
| A.需要加热才能发生的反应一定是吸热反应 |
| B.放热反应在常温下一定很容易发生 |
| C.反应是放热还是吸热,可根据反应物和生成物所具有的总能量的相对大小判断 |
| D.吸热反应在常温下一定不能发生 |