在一固定容积的密闭容器中进行着如下反应: CO2(g) + H2(g) 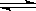 CO(g) + H2O(g) 其平衡常数K和温度t的关系如下:
CO(g) + H2O(g) 其平衡常数K和温度t的关系如下:
| t℃ |
700 |
800 |
850 |
1000 |
1200 |
| K |
2.6 |
1.7 |
1.0 |
0.9 |
0.6 |
(1)该反应的逆反应为 反应(“吸热”或“放热”);
(2)不能判断该反应是否已经达到化学平衡状态的是:
A.容器中压强不变 B.混合气体中CO浓度不变
C.v(H2)正 = v(H2O)逆 D.c(CO2) = c(CO)
(3) 在850℃时,可逆反应:CO2(g) + H2(g) 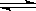 CO(g) + H2O(g),在该容器内各物质的浓度变化如下:
CO(g) + H2O(g),在该容器内各物质的浓度变化如下:
| 时间/min |
CO2 (mol/L) |
H2 (mol/L) |
CO (mol/L) |
H2O ( mol/L) |
| 0 |
0.200 |
0.300 |
0 |
0 |
| 2 |
0.138 |
0.238 |
0.062 |
0.062 |
| 3 |
c1 |
c2 |
c3 |
c3 |
| 4 |
c1 |
c2 |
c3 |
c3 |
计算:3min—4min达到平衡时CO的平衡浓度c3和CO2 (g)的转化率,要求写出简单的计算过程(c3精确到小数点后面三位数)。
W,X,Y,Z四种短周期元素,原子序数依次增大,在周期表中W与X相邻、Y与Z相邻.已知W元素的氢化物与Z元素的氢化物反应只生成一种盐a;X,Y位于同一族,它们能组成YX2,YX3两种常见化合物.请回答下列问题:
(1)X元素位于周期表的位置为_____________________________________
(2)X,Y,Z三种元素形成的单质中,氧化性最弱的是___________(填化学式).
(3)a溶液的pH__________7(填“>”、“<”或“=”),用离子方程式解释为:__________.
(4)Y与Z可形成共价化合物Y2Z2,分子中Y与Z均满足8电子稳定结构,则Y2Z2的电子式为__________.Y2 Z2遇水很易反应,产生的气体能使品红溶液褪色,则其与水反应的化学方程式为______________________
(5)工业上用氧化WH3法制取WO,该反应的热化学方程式为:
4WH3(g)+5O2(g)=4WO(g)+6H2O(g) △H=-905.8kJ·mol-1;
已知W2(g)+O2(g)=2WO(g) △H="+180" kJ·mol-1,则WH3与氧气反应产生两种无污染物质的热化学方程式为 。
将等物质的量的A、B混合于2 L的密闭容器中,发生如下反应:
3A(g)+B(g)  xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min)。求:
xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min)。求:
(1)此时A的浓度c(A)=________mol/L,反应开始前容器中的A、B的物质的量:
n(A)=n(B)=________mol。
(2)B的平均反应速率v(B)=________mol/(L·min)。
(3)x的值为________。
早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成。回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过 方法区分晶体、准晶体和非晶体。
(2) 基态Fe原子有 个未成对电子,Fe3+的电子排布式为 。可用硫氰化钾检验Fe3+,形成的配合物的颜色为 。
(3) 新制备的Cu(OH)2可将乙醛(CH3CHO)氧化为乙酸,而自身还原成Cu2O,乙醛中碳原子的杂化轨道类型为 ,1mol乙醛分子中含有的σ键的数目为 。乙酸的沸点明显高于乙醛,其主要原因是 。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有 个铜原子。
(4)Al单质为面心立方晶体,其晶胞参数a=0.405nm,晶胞中铝原子的配位数为 。列式表示Al单质的密度 g·cm-3(不必计算出结果)
普通纸张的主要成分是纤维素,在早期的纸张生产中,常采用纸表面涂覆明矾的工艺,以填补其表面的微孔,防止墨迹扩散,请回答下列问题:
(1)人们发现纸张会发生酸性腐蚀而变脆、破损,严重威胁纸质文物的保存。经分析检验,发现酸性腐蚀主要与造纸中涂覆明矾的工艺有关,其中的化学原理是 ;为了防止纸张的酸性腐蚀,可在纸浆中加入碳酸钙等添加剂,该工艺原理的离子方程式为 。
(2)为了保护这些纸质文物,有人建议采取下列措施:
①喷洒碱性溶液,如稀氢氧化钠溶液或氨水等,这样操作产生的主要问题是 。
②喷洒Zn(C2H5)2。Zn(C2H5)2可以与水反应生成氧化锌和乙烷。用化学(离子)方程式表示该方法生成氧化锌及防治酸性腐蚀的原理 。
(3)现代造纸工艺常用钛白粉(TiO2)替代明矾。钛白粉的一种工业制法是以钛铁矿(主要成分FeTiO3)为原料按下列过程进行的,请完成下列化学方程式:
①_____FeTiO3+_____C+_____Cl2 _____TiCl4+_____FeCl3+_____CO
_____TiCl4+_____FeCl3+_____CO
②____TiCl4+ ____O2 ____TiO3+____Cl2
____TiO3+____Cl2
减少污染、保护环境是全世界最热门的课题。
I.CO在催化剂作用下可以与H2反应生成甲醇:
①CO(g)+2H2(g)  CH3OH(g),△H1
CH3OH(g),△H1
(1)已知反应①中的相关的化学键键能数据如下:
| 化学键 |
H-H |
C-O |
 C O C O |
H-O |
C-H |
| E/(kJ·mol-1) |
436 |
343 |
876 |
465 |
413 |
由此计算△H1= 。
(2)图1中能正确反映反应①平衡常数的对数lgK随反应温度T的变化曲线为 (填曲线标记字母),其判断理由是 。

(3)在密闭容器中充有10 mol CO与20 mol H2,CO的平衡转化率与温度、压强的关系如图2。
①P1 P2(填“大于”或“小于”),其判断理由是 。
②M、N、Q三点平均速率ν(M)、ν(N)、ν(Q)大小关系为 。
③M、N、Q三点平衡常数KM、KN、KQ大小关系为 。
II.一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g) 2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示。已知:气体分压(P分)= 气体总压(P总)× 体积分数。
2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示。已知:气体分压(P分)= 气体总压(P总)× 体积分数。
完成下列填空:
①650℃时,反应达平衡后CO2的转化率为 。
②T℃时,若充入等体积的CO2和CO,平衡 (填“向左移动”、“向右移动”或“不移动”)
③925℃时,P总=1/96MPa,用平衡分压代替平衡浓度表示的化学平衡常数KP= 。