为了达到下表中的实验要求,请从供选择的化学试剂及实验方法中选出合适的,将其标号填入对应的空格中。
| 题号 |
实验要求 |
答案 |
| (1) |
从碘水中提取碘单质 |
|
| (2) |
提纯混有少混NaCl的KNO3 |
|
| (3) |
鉴别NaCl和KCl |
|
| (4) |
测定某工业废水的酸碱度 |
|
| (5) |
检验自来水中残余氯分子 |
|

净水丸能对饮用水进行快速的杀菌消毒,药丸通常分内外两层。外层的优氯净[Cl2Na(NCO)3,氯元素为+1价]先与水反应,生成次氯酸(HClO)起杀菌消毒作用;几分钟后,内层的亚硫酸钠(Na2SO3)溶出,可将水中的余氯(次氯酸)除去。
(1)优氯净中氮元素的化合价为 。
(2)亚硫酸钠将水中多余次氯酸除去的离子反应方程式为 。
(3)亚硫酸钠溶液在空气中易变质,请写出检验亚硫酸钠溶液是否变质的方法 。
四种短周期元素W、X、Y、Z,原子序数依次增大,请结合表中信息回答下列问题。
| W |
X |
Y |
Z |
|
| 结构 或性质 |
最高价氧化物对应的水 化物与其气态氢化物反 应得到离子化合物 |
焰色反应呈黄色 |
在同周期主族元素形成的简单离子中,离子半径最小 |
最高正价与最 低负价之和为6 |
(1)W元素和氢可形成离子化合物,其电子式为 。
(2)Y元素和Z元素可形成YZ3化合物,可用于净水剂,净水原理 (用离子方程式表示)。
(3)①下列可作为比较X和Y金属性强弱的依据是 (填序号)。
a.最高价氧化物的水化物能反应 b.相应硫酸盐水溶液的pH
c.单质与水反应的难易程度 d.单质与酸反应时失去的电子数
②由X、Y、氢、氧四种元素所组成的化合物,能与盐酸以1:4反应生成两种常见盐和水,则该化合物的化学式为 。
(4)W的一种氢化物HW3可用于有机合成,其酸性与醋酸相似。体积和浓度均相等的HW3与X的最高价氧化物对应的水化物混合,混合后溶液中离子浓度由大到小的顺序是 。
现有反应CO(g)+2H2(g) CH3OH(g)过程中能量变化如下图所示,写出该反应的热化学方程式 ;
CH3OH(g)过程中能量变化如下图所示,写出该反应的热化学方程式 ;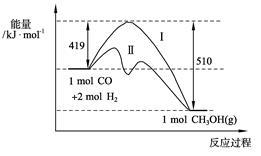
已知该反应中相关的化学键键能数据如下:
| 化学键 |
H—H |
C—O |
H—O |
C—H |
| E/(kJ·mol-1) |
436 |
343 |
465 |
413 |
则C≡O中的键能为 KJ·mol-1;图中曲线Ⅱ表示 (填反应条件)的能量变化。
实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低,最低可以还原到-3价。某同学取一定量的铁铝合金与一定量很稀的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入4 mol·L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。试回答下列问题: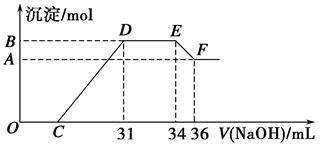
(1)请写出该合金中铁与硝酸反应的离子方程式 。
(2)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为 。
(3)在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为 。
(4)B与A的差值为 mol。
(5)B点对应的沉淀的物质的量为 mol,C点对应的氢氧化钠溶液的体积为_____ mL。
常见的五种盐A、B、C、D、E,它们的阳离子可能是Na+、NH4+、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、NO3-、SO42-、CO32-,已知:
①五种盐均溶于水,水溶液均为无色。
②D的焰色反应呈黄色。
③A的溶液呈中性,B、C、E的溶液呈酸性,D的溶液呈碱性。
④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有A、C的溶液不产生沉淀。
⑤若在这五种盐的溶液中,分别加入氨水,E和C的溶液中生成沉淀,继续加氨水,C中沉淀消失。
⑥把A的溶液分别加入到B、C、E的溶液中,均能生成不溶于稀硝酸的沉淀。
请回答下列问题。
(1)五种盐中,一定没有的阳离子是 ;所含阴离子相同的两种盐的化学式是 。
(2)D的化学式为 ,D溶液显碱性的原因是(用离子方程式表示) 。
(3)A和C的溶液反应的离子方程式是 ;E和氨水反应的离子方程式是 。
(4)若要检验B中所含的阳离子,正确的实验方法是 。