(每空2分,共8分)某有机物完全燃烧生成标准状况下CO2的体积为4.48L,H2O的质量为5.4g,
(1)若此有机物的质量为3g,则此有机物的结构简式是______________________;
(2)若此有机物的质量为4.6g,则此有机物的结构简式是____________________;
(3)若此有机物的质量为6.2g,且此有机物1mol能和金属钠反应生成1molH2,则此有机物的结构简式是__________________;
(4) 等物质的量的此三种有机物完全燃烧,消耗氧气最多的是(名称)____________。
主族元素W、X、Y、Z的原子序数依次增大,W的原子最外层电子数是次外层电子数的3倍。X、Y和Z分属不同的周期,它们的原子序数之和是W原子序数的5倍。在由元素W、X、Y、Z组成的所有可能的二组分化合物中,由元素W与Y形成的化合物M的熔点最高。请回答下列问题:
(1)W元素原子的L层电子排布式为,W3分子空间构型为;
(2)X单质与水发生主要反应的化学方程式为;
(3)化合物M的化学式为,其晶体结构与NaCl相同,而熔点高于NaCl。M熔点较高的原因是。将一定量的化合物ZX负载在M上可制得ZX/M催化剂,用于催化碳酸二甲酯与月桂醇酯交换合成碳酸二月桂酯。在碳酸二甲酯分子中,碳原子采用的杂化方式有,O—C—O的键角约为;
(4)X、Y、Z可形成立方晶体结构的化合物,其晶胞中X占据所有棱的中心,Y位于顶角,Z处于体心位置,则该晶体的组成为X:Y:Z=;
(5)含有元素Z的盐的焰色反应为色。许多金属盐都可以发生焰色反应,其原因是。
研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学方程式为;利用反应6NO2+ 8NH3 7N5+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是L。
7N5+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是L。
(2)已知:2SO2(g)+O2(g) 2SO3(g)
2SO3(g)
ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g) 2NO2(g)
2NO2(g)
ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH=kJ·mol-1。一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是。
SO3(g)+NO(g)的ΔH=kJ·mol-1。一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO3的同时生成1 molNO2
测得上述反应平衡时NO2与SO2体积比为1:6,则平衡常数K=。
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g) CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图所示。该反应ΔH0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图所示。该反应ΔH0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是。
物质A ~G有下图所示转化关系(部分反应物、生成物没有列出)。其中A为某金属矿的主要成分,经过一系列反应可得到B和C。单质C可与E的浓溶液发生反应,G为砖红色沉淀。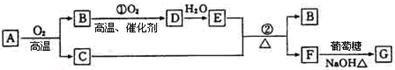
请回答下列问题:
(1)写出下列物质的化学式:B、E、G;
(2)利用电解可提纯C物质,在该电解反应中阳极物质是,阴极物质是,电解质溶液是;
(3)反应②的化学方程式是;
(4)将0.23molB和0.11mol氧气放入容积为1L的密闭容器中,发生反应①,在一定温度下,反应达到平衡,得到0.12molD,则反应的平衡常数K=。若温度不变,再加入0.50mol氧气后重新达到平衡,则B的平衡浓度(填“增大”、 “不变”或“减小”),氧气的转化率(填“升高”、“不变”或“降低”),D的体积分数(填“增大”、“不变”或“减小”)。
.电炉加热时用纯氧气氧化管内样品,根据产物的质量确定有机物的组成,下列装置是用燃烧法确定有机物分子式常用的装置(E中电炉省去)。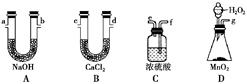
(1)产生的氧气按从左到右的流向,所选装置各导管的连接顺序是__________________。
(2)C装置中浓H2SO4的作用是__________________。
(3)D装置中MnO2的作用是____________________。
(4)E燃烧管中CuO的作用是______________________。
(5)若准确称取0.90 g样品(只含C、H、O三种元素中的两种或三种),经充分燃烧后,A管质量增加1.32 g,B管质量增加0.54 g,则该有机物的最简式为_____________________ (3分)。
(6)要确立该有机物的分子式,还要知道________________________________________。
.随着现代工业的发展,能源问题已经越来越引起人们的重视,科学家预言,未来最理想的燃料是绿色植物,即将植物的秸秆(主要成分是纤维素)用适当的催化剂可以水解成葡萄糖,再将葡萄糖转化为乙醇,用做燃料。
(1)写出绿色植物的秸秆转化为乙醇的化学方程式:
①____________________________________
②________________________________________。
(2)乙醇除用做燃料外,还可以用它合成其他有机物,以乙醇为起始原料的转化关系如图所示:(已知;在有催化剂的条件下,多步氧化R-CH2OH→R-CHO→RCOOH)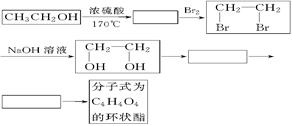
请在方框中填上相应物质的结构简式。
(3)写出上面转化关系图中由CH2OHCH2OH―→C4H4O4的化学方程式(有机物用结构简式表示)。