设NA为阿伏加德罗常数的值, 下列叙述正确的是
下列叙述正确的是
A.常温常压下, 2.8g N2与C2H 4的混合气体所含电子数为1.4 NA 4的混合气体所含电子数为1.4 NA |
| B.标准状况下,1.12 L NO与1.12O2的混合物中含有的原子数为0.2NA |
C.25℃时,pH=13的 Ba(OH)2溶液中含有的OH-数目为0.1  NA NA |
| D.常温下,1 L 0.1 mol·L-1的NH4NO3溶液中氧原子数为0.3 NA |
实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是()
| 选项 |
a中物质 |
b中物质 |
c中收集气体 |
d中物质 |
| A |
浓氨水 |
CaO |
NH3 |
H2O |
| B |
浓硫酸 |
浓盐酸 |
HCl |
NaOH溶液 |
| C |
稀硝酸 |
Cu |
NO2 |
H2O |
| D |
浓盐酸 |
MnO2 |
Cl2 |
NaOH溶液 |
X、Y、Z、W四种短周期元素在周期表中的相对位置如右图所示,其中X与W的质子数之和为21,由此可知()
| X |
Y |
||
| Z |
W |
A.X位于元素周期表中第2周期、第VA族
B.Y的氢化物(H2Y)不稳定,100℃以上即可分解
C.Z的最高价氧化物的水化物是一种强碱
D.W的非金属性比Y的非金属性弱
下列图像表达正确的是()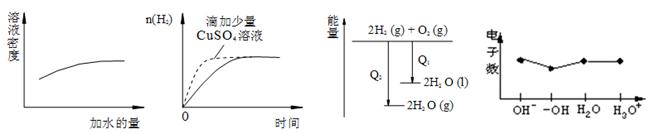
| A.浓硫酸的稀释等量的锌粉反应 | B.过量的盐酸与能量变化 |
| C.氢气与氧气反应中的 | D.微粒电子数 |
下列离子方程式错误的是()
| A.向Mg(HCO3)2溶液中加入过量的 NaOH溶液:Mg2++2HCO3-+4OH-=Mg(OH)2↓+2CO32-+2H2O |
| B.向亚硫酸钡固体中加入稀硝酸:3BaSO3+2H++2NO3-=3BaSO4↓+2NO↑+H2O |
| C.在银氨溶液中滴加过量稀硝酸:[Ag(NH3)2]++2H+ = Ag++2NH4+ |
| D.向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至SO42-刚好沉淀完全: |
Ba2+ + 2OH-+ NH4+ + H+ + SO4 2-= BaSO4↓+ NH3·H2O + H2O
据报道,科学家发现了如下反应:O2+PtF6=O2(PtF6),已知O2(PtF6)为离子化合物,其中Pt为+5价,对于此反应,下列说法正确的是()
| A.O2(PtF6) 中不存在共价键 |
| B.在此反应中每生成1mol O2(PtF6)则转移lmol电子 |
| C.O2(PtF6)中氧元素的化合价是+l价 |
| D.在此反应中,O2是氧化剂,PtF6是还原剂 |