下列离子方程式正确的是( )
| A.向CaCl2溶液中通入少量CO2: Ca2+ + CO2 + H2O = CaCO3↓+ 2H+ |
| B.FeBr2溶液与等物质的量的Cl2反应:2Fe2+ +2Br - +2Cl2=2Fe3+ +4Cl-+Br2 |
| C.Fe3O4与稀硝酸反应:2Fe3O4 +18H+=6Fe3+ +H2↑+8H2O |
| D.向次氯酸钙溶液通入少量SO2:Ca2++ 2ClO- + SO2+ H2O = CaSO3↓ + 2HClO |
下列说法中正确的是()
A.凡是放热反应都是自发的,吸热反应都是非自发的
B.在反应A(g)+3B(g)=2C(g)+2D(g) 的速率测定实验中,分别测得反应速率如下:v(A)=0.15mol·L—1·s—1 , v(C)=0.3 mol·L—1·s—1 ,则用C来表示反应进行的速率更快
C.反应HCl( aq ) + NaOH( aq )=NaCl( aq ) + H2O( l ) △H<0,在理论上能用于设计原电池
D.如下图所示,在一U型管中装入含有紫色石蕊试液的Na2SO4溶液,通直流电,一段时间后U型管内会形成一个倒立的三色“彩虹”,从左到右颜色的次序是.红、紫、蓝
在一定条件下,恒容的密闭容器中发生如下反应:2SO2 (g)+O2(g) 2SO3(g),反应过程中某一时刻测得SO2、O2、SO3的浓度分别为0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1,当反应达到平衡时,可能出现的数据是()
2SO3(g),反应过程中某一时刻测得SO2、O2、SO3的浓度分别为0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1,当反应达到平衡时,可能出现的数据是()
| A.C(SO3)=0.4mol·L-1 | B.C(SO3)=C(SO2)="0.15" mol·L-1 |
| C.C(O2)=0.3mol·L-1 | D.C(SO3)+C(SO2)="0.4" mol·L-1 |
关于下列装置说法正确的是 ( )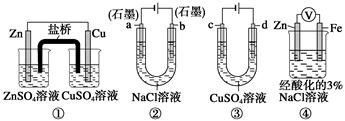
| A.装置①中,盐桥中的K+移向ZnSO4溶液 |
| B.装置②工作一段时间后,a极附近溶液的OH–的浓度增大 |
| C.用装置③精炼铜时,c极为粗铜 |
| D.装置④中电子由Zn流向Fe,装置中有Fe2+生成 |
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
| A.放电时负极反应为:Zn-2e-+2OH-===Zn(OH)2 |
B.充电时阳极反应为:Fe(OH)3-3e-+5OH-===FeO +4H2O +4H2O |
| C.放电时每转移3 mol 电子,正极有1 mol K2FeO4被氧化 |
| D.放电时正极附近溶液的碱性增强 |
在体积一定的密闭容器中给定物质A、B、C的量,在一定条件下发生反应建立的化学平衡:aA(g) + bB(g) cC(g),符合下图所示的关系(c%表示混合气中产物C的百分含量,T表示温度,p表示压强,t表示时间)。在图中,Y轴是指()
cC(g),符合下图所示的关系(c%表示混合气中产物C的百分含量,T表示温度,p表示压强,t表示时间)。在图中,Y轴是指()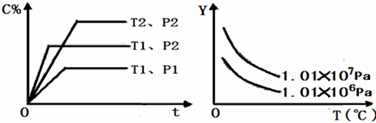
A.平衡混合气中物质A的百分含量B.平衡混合气中物质B的百分含量
C.平衡混合气的平均摩尔质量D.平衡混合气的密度