反应:L(s)+aG(g) bR(g) 达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数。据此可判断
bR(g) 达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数。据此可判断
A.a>b 上述反应是放热反应
B.a < b 上述反应是吸热反应
C.a>b 上述反应是吸热反应
D.a < b 上述反应是放热反应
对于等物质的量浓度的Na2CO3和NaHCO3溶液,下列说法不正确的是
| A.分别升高温度,两种溶液的pH均减小 |
| B.相同温度下两种溶液的pH:Na2CO3> NaHCO3 |
| C.分别加少量NaOH,两液c(CO32-)均增大 |
| D.两液均存在c(Na+) + c(H+)=c(OH-) + c(HCO3-) + 2c(CO32-) |
关于下图所示的原电池,下列说法正确的是 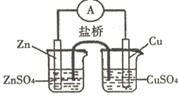
| A.电子从锌电极通过电流表流向铜电极 |
| B.盐桥中的阴离子向硫酸铜溶液中迁移 |
| C.取出盐桥后,电流计的指针仍发生偏转 |
| D.铜电极上发生的电极反应是2H+ + 2e- = H2↑ |
标准状态下,在四个干燥的烧瓶中分别充入:① 纯净的氨气,② 混有1/3体积空气的氯化氢气体,③ 纯净的NO2气体,④ 混有少量O2的NO2气体。然后各做喷泉实验。实验后,三烧瓶中溶液的物质的量浓度大小关系是
| A.①=②=③=④ | B.①=②=③>④ | C.①=②=③<④ | D.④>①=②>③ |
在下列溶液中,各组离子一定能够大量共存的是
| A.pH=2的溶液:Fe3+、Cu2+、SO42-、NO3- |
| B.c(H+)=1×10-12mol/L的溶液:NH4+、K+、Cl-、AlO2- |
| C.水电离的c(H+)=1×10-12mol/L的溶液:Na+、Al3+、Br-、ClO- |
| D.与铝反应放出氢气的溶液:Na+、Mg2+、Br-、Cl- |
绿原酸的结构简式如图,下列有关绿原酸的说法不正确的是
| A.分子式为C16H18O9 |
| B.能与Na2CO3反应 |
| C.能发生取代反应和消去反应 |
| D.0.1 mol绿原酸最多与0.8 mol NaOH反应 |