常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表,请回答:
| 实验编号 |
HA物质的量浓度(mol·L-1) |
NaOH物质的量浓度(mol·L-1) |
混合溶液的pH |
| 甲 |
0.2 |
0.2 |
pH=a |
| 乙 |
c |
0.2 |
pH=7 |
| 丙 |
0.2 |
0.1 |
pH>7 |
| 丁 |
0.1 |
0.1 |
pH=9 |
(1)不考虑其它组的实验结果,单从甲组情况分析,如何用a (混合溶液的pH)来说明HA是强酸还是弱酸________。
( 2)不考虑其它组的实验结果,单从乙组情况分析,C是否一定等于0.2________(选填“是”或“否”)。混合液中离子浓度c(A-)与 c(Na+)的大小关系是__________
2)不考虑其它组的实验结果,单从乙组情况分析,C是否一定等于0.2________(选填“是”或“否”)。混合液中离子浓度c(A-)与 c(Na+)的大小关系是__________
(3)丙组实验结果分析,HA是________酸(选填“强”或“弱”)。该混合溶液中离子浓度由大到小的顺序是________________________________
(4)丁组实验所得混合溶液中由水电离出的c(OH-)=________mo l·L-1。
l·L-1。
某小组以醋酸为例探究弱酸的性质。
(1)实验一:探究酸的强弱对酸与镁条反应速率的影响。
①设计实验方案如下表,表中c =________mol·L-1。
| 编号 |
酸的种类 |
酸的浓度/mol·L-1 |
酸的体积/mL |
镁条质量/g |
| 1 |
醋酸 |
1.0 |
10 |
2.0 |
| 2 |
盐酸 |
c |
10 |
2.0 |
②实验步骤:a)检查装置(如图)的气密性后,添加药品;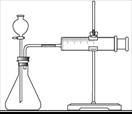
b)反应开始后,________;
c)将所记录的数据转化为曲线图(下图).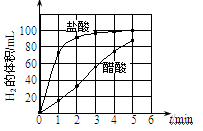
③写出0~5min醋酸、盐酸与镁条反应的反应速率变化规律:________。
(2)实验二:现有一瓶醋酸溶液,常温下测定其中醋酸的电离程度(已电离的电解质分子数占原来总分子数的百分比)。设计实验方案,将待测物理量和对应的测定方法填写在下表中。
| 待测物理量 |
测定方法 |
| ①__________ |
量取25.00ml醋酸溶液于锥形瓶中,滴加指示剂,将0.1000mol·L-1 NaOH标准溶液装入________,滴定至终点,记录数据.重复滴定2次. |
| ②__________ |
__________ |
氯化法是合成硫酰氯(SO2Cl2)的常用方法,实验室合成硫酰氯(SO2Cl2)的反应和实验装置如下:SO2(g)+Cl2(g)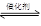 SO2Cl2(l) △H=-97.3kJ/mol。
SO2Cl2(l) △H=-97.3kJ/mol。
有关信息如下:硫酰氯通常条件下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中“发烟”;100℃以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解。回答下列问题:
(1)装置甲中仪器A的名称为______,甲中活性炭的作用是________,B的作用为;
(2)装置丁中发生反应的离子方程式为;
(3)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯与另外一种物质,该反应的化学方程式为,分离产物的方法是(填字母);
| A.重结晶 | B.过滤 | C.蒸馏 | D.萃取 |
(4)装置丙的作用为,若缺少装置乙,氯气和二氧化硫可能发生反应的化学方程式为;
(5)为提高本实验中硫酰氯的产率,在实验操作中需要注意的事项有(填序号)。
①先通冷凝水,再通气 ②控制气流速率,宜慢不宜快
③若三颈烧瓶发烫,可适当降温 ④加热三颈烧瓶
冰晶石是一种矿物,主要成分为六氟合铝酸钠(Na3AlF6),微溶于水,熔融的冰晶石能溶解氧化铝,在电解铝工业作助熔剂,制造乳白色玻璃和搪瓷的遮光剂。工业上生产Na3AlF6的主要流程如下: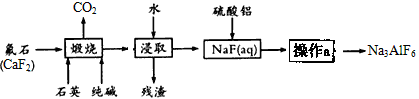
试结合生产流程回答下列问题:
(1)浸取后的“残渣”中一定含有的成分是________,硫酸铝与NaF(aq)反应的离子方程式为____;
(2)为提高NaF的浸出率,煅烧后的固体在浸取前应采取的措施为,为得到纯净的Na3AlF6产品,操作a包括的主要操作步骤为→→;
(3)在按化学计量加入硫酸铝溶液前,需先用硫酸将NaF(aq)的pH下调至5左右,请解释其原因是;
(4)78kg含CaF280%的氟石(杂质不含氟元素)理论上可生产Na3AlF6______kg(设生产过程中的每一步含氟物质均完全转化);
(5)碳酸化法也是工业制取Na3AlF6的一种方法:在偏铝酸钠及氟化钠溶液中,通入足量二氧化碳即可,请写出该反应的化学方程式_____________。
实验室用溴化钠、浓硫酸和醇制备溴乙烷(CH3CH2Br)和1—溴丁烷(CH3CH2CH2CH2Br)的反应原理如下
可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br-被浓硫酸氧化为Br2等。有关数据列表如下:
请回答下列问题:
(1)溴乙烷和1-溴丁烷的制备实验中,下列仪器最不可能用到的是。(填字母)
a.圆底烧瓶b.量筒c.温度计d.普通漏斗
(2)制备实验中常采用80%的硫酸而不用98%的浓硫酸,其主要原因是。
(3)在制备溴乙烷时,采用边反应边蒸出产物的方法,这样有利于;但在制备1-溴丁烷时却不能边反应边蒸出产物,其原因是。
(4)将制得的1-溴丁烷粗产品置于分液漏斗中,依次加入NaHSO3溶液和水,振荡、静置后,
1-溴丁烷在(填“上层”、“下层”或“不分层”),加入NaHSO3溶液的目的是。
(5)将实验(4)所得的1-溴丁烷粗产品干燥后,进行操作,即可得到纯净的1-溴丁烷。
(6)某实验小组在制取1-溴丁烷的实验中所取1-丁醇(CH3CH2CH2CH2OH)7.4 g.NaBr13.0 g,最终制得1-溴丁烷9.6 g,则1-溴丁烷的产率是。(保留2位有效数字)
某学习小组设计实验,探究二氧化硫的漂白性和还原性。
(1)漂白性
甲同学用如图所示装置(气密性良好)进行实验,观察到如下现象:Ⅰ中红色褪去,Ⅱ中无变化。
①甲同学作对照实验的目的是。
②足量碱石灰的作用是。
甲同学由此得出的实验结论是。
(2)还原性:
乙同学将SO2通入FeCl3溶液中,使其充分反应。
①SO2与FeCl3反应的离子方程式是,检验该反应所得含氧酸根离子的方法是。
②实验中观察到溶液由黄色变为红棕色,静置一段时间,变为浅绿色。资料显示:红棕色为FeSO3 (墨绿色难溶物)与FeCl3溶液形成的混合色。 则②中红棕色变为浅绿色的原因是。
乙同学得出的实验结论是:二氧化硫可还原三氯化铁。