一定条件下,体积为10L的密闭容器中,1molX和1molY进行反应:2X(g)+Y(g) Z(g),经60s达到平衡,生成0.3molZ。下列说法正确的是
Z(g),经60s达到平衡,生成0.3molZ。下列说法正确的是
A.若增加X的浓度,则 Z的质量分数一定增大 Z的质量分数一定增大 |
B.将容器体积变为20L,Z的平衡浓度变为原来的 |
| C.若增大压强,则物质Y的转化率减小 |
| D.若升高温度,X的浓度增大,则该反应的△H<0 |
下列有关生活中的化学叙述不正确的是()
| A.目前国内销售的加碘食盐中加入的是KIO3 |
| B.向燃料煤中加入生石灰,可减少对大气的污染 |
| C.食用植物油的主要成分是高级饱和脂肪酸的甘油酯,是人体不可缺少的营养物质 |
| D.洗涤剂去油脂主要是物理变化,碱液去油脂属于化学变化 |
下列物质中既不能发生水解反应也不能发生还原反应的是()
| A.葡萄糖 | B.纤维素 | C.乙醇 | D.蔗糖 |
将1.62g淀粉在一定条件下水解,反应一段时间后,向容器中加入足量的银氨溶液,结果析出0.108g银,则淀粉的水解率为 ( )
| A. 8% | B. 10% | C. 5% | D.无法计算 |
具有一个醇羟基的有机物A与8g乙酸充分反应生成了10.2g乙酸乙酯,经分析还有2g乙酸剩余,下列醇中有可能是A的是()
A.C2H5OH B.C6H5—CH2—OH
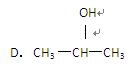
下列物质中,可一次性鉴别乙酸、乙醇、苯及氢氧化钡溶液的是()
| A.金属钠 | B.溴水 | C.碳酸钠溶液 | D.紫色石蕊溶液 |