(7分)空气、水是人类赖以生存的自然资源。
(1)测定空气中氧气体积分数的实验装置如下图所示。在集气瓶内加入少量的水,并五等分水面以上容积,做上记号。用弹簧夹夹紧乳胶管。点燃燃烧匙内足量的红磷,立即伸入瓶中并把塞子塞紧。
①写出红磷在空气中燃烧的化学方程式:
②待红磷熄灭并冷却后,打开弹簧夹,观察到烧杯中的水进入集气瓶,瓶内水面最终 上升约至1刻度处。由此可知氧气约占空
上升约至1刻度处。由此可知氧气约占空 气总体积的 。
气总体积的 。
③红磷熄灭后,集气瓶内剩下的气体主要是 (填“支持”或“不支持”)燃烧
(2)某含有许多可溶性和不溶性杂质的天然水,经吸附、沉淀、过滤等初步净化处理后,再加热煮沸,在盛水的器具上会有水垢生成,则这种煮沸前经初步净化处理后的水
是 (填“软水”或“硬水”)。
(3)下列对有关水资源认识的叙述中 ,错误的是
,错误的是
| A.水体污染加剧了淡水资源危机 |
| B.节约用水是每个公民应尽的义务 |
| C.地球表面约71%被水覆盖,可利用的淡水资源十分丰富 |
| D.天津属极度缺水的地区,可以考虑通过海水淡化来解决用水问题 |
硝酸钾是初中化学常见的一种物质。请按要求填空:
(1)质量分数为4.04%的硝酸钾(KNO3)溶液可作为无土栽培的营养液。该营养液(填“属于”或“不属于”)复合肥;
(2)在硝酸钾溶液中,共有三种微粒,它们是K+、NO3-和(用符号表示);
(3)黑火药爆炸的反应原理是:2KNO3+S+3C K2S+3CO2↑+N2↑,此反应的反应物和生成物中,没有涉及到下列物质类别中的(填序号)
K2S+3CO2↑+N2↑,此反应的反应物和生成物中,没有涉及到下列物质类别中的(填序号)
| A.单质 | B.氧化物 | C.酸 | D.碱 E.盐 |
(4)如右图,硝酸钾的溶解度随温度的升高而,50℃时,硝酸钾和氯化钠饱和溶液降温至20℃后,硝酸钾的溶质质量分数氯化钠的溶质质量分数(填“﹥”、“﹦”或“﹤”),欲将接近饱和的 KNO3溶液变成饱和溶液,可采取的方法有(列举一种)。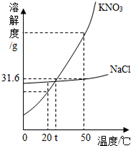
金属材料在工业上有广泛的用途。
(1)铝合金材质与纯铝比较,主要优点是;
(2)钢铁的锈蚀主要是铁与空气中的共同作用的结果,工业生产中常用稀盐酸除去铁制品表面的铁锈,该反应的化学方程式为;
(3)为了避免钢铁腐蚀,通常在钢铁外壳上镶嵌比铁活动性强的金属。小明为探究锌、铁、铜三种金属的活动性顺序,设计了如图的两个实验: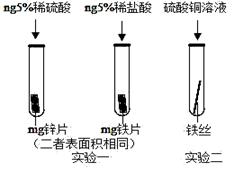
①实验一,小明以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为不够合理,理由是;②实验二,若出现现象,可证明铁的活动性强于铜,该反应的化学方程式为。
化学是以实验为基础的科学。根据所学知识,完成下列问题。
(1)实验A中标号为①的仪器名称是,实验A制取氧气发生的化学方程式为;
(2)实验B的操作是违规的,正确方法是;
(3)实验C中烧杯③的作用是;
(4)实验D中,气球的变化情况是先变大后变小,写出导致气球变小的化学方程式。
请根据要求填空:
(1)汽车尾气装置发生的反应是:2NO+2CO→N2+2CO2,该反应的基本类型是;
| A.化合反应 | B.分解反应 | C.置换反应 | D.复分解反应 E.不属于上述中的一种 |
(2)DNA水解产物中的胸腺嘧啶(C3H6N2O2),该物质中氮元素与氧元素的质量比为;
(3)可燃冰的主要成分是甲烷(CH4),写出其燃烧的化学反应方程式。
碘元素是人体必需的微量元素之一。
(1)下图是元素周期表中碘元素的部分信息。碘原子的核电荷数是,
碘元素属于(填“金属”或“非金属”)元素;
(2)已知某碘盐的主要成分为氯化钠和碘酸钾(KIO3)。
①氯化钠中含有的阴离子是(用符号表示),KIO3中I的化合价为价;
②用试剂X测定该碘盐中碘元素的含量,发生如下反应:
KIO3+5X+3H2SO4=3K2SO4+3I2+3H2O,推算X的化学式为。