已知五种短周期元素在周期表中的相对位置如下表所示。
| A |
|
|
|
|
|
| |
|
|
|
|
B |
| c |
|
d |
|
|
e |
(1)上述元素中离子半径最大的是_______________(填写元素符号)。
(2)已知A、B、C、D、E五种化合物均由上述元素中的几种组成。它们之间的转换关系如图所示,且A、B、E三种物质含有相同的一种金属元素,C和D分别是常见的强酸和强碱,则:①A、B、E所含的该金属元素的原子结构示意图为_________________________________________;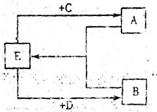
②若将D逐滴滴入A的溶液中至过量,反应过程中的离子方程式依次为______________________________________________________________。
【 化学一物质结构与性质 】
(1)已知X、Y、Z为同一短周期的三种元素,其原子的部分电离能(kJ/mol)如下表所示:
| X |
Y |
Z |
|
| I1 |
496 |
738 |
577 |
| I2 |
4562 |
1451 |
1817 |
| I3 |
6912 |
7733 |
2754 |
| I4 |
9540 |
10540 |
11578 |
①三种元素电负性大小关系为_______________
②写出Y原子的电子排布式_____________ Y的第一电离能大于Z的第一电离能的原因________________
③X晶体采用下列_________(填字母) 堆积方式。
A B C D
(2)N第一电离能也反常,导致它的一些性质也出现反常。已知N—N、N=N、N≡N键能之比为1.00:2.17:4.90,而C—C、C=C、C≡C键能之比为1.00:1.77:2.34,由此你得出的结论是:____________________。
(3)N2O的等电子体为:①分子______________,②阴离子______________;由此可知N2O的中心原子的杂化类型为________。根据价层电子对互斥模型确定NO2的分子构型为: ________________。
(4)已知铜能形成多种化合物,如硫酸铜的结构如下图所示,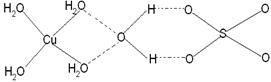
请在图中标出水合铜离子中的配位键.
【化学一化学与技术】
氮的化合物及相关工业的生产路线如下图所示: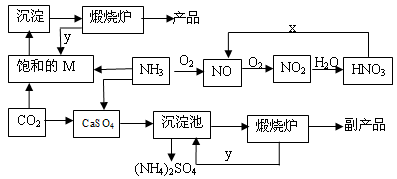
(1)M的化学式为____________;循环利用的物质y为__________________。
(2)产品的俗称是______________;副产品的俗称为______________________。
(3)若x为亮红色的单质,请写出硝酸与x反应生成NO 的离子方程式: _______________
(4)向装有CaSO4悬浊液的沉淀池中先通氨气,再通CO2的原因是。
(I)阅读下面信息,推断元素,按要求回答问题:
| 信息 |
问题 |
| ①短周期元素X、Y、Z、W,原子序数依次增大, 最外层电子数均不少于最内层电子数 |
⑴仅针对信息①,X一定不是 A.氢 B.碳C.氧 D.硫 |
| ②一定条件下,上述四种元素的单质均能与足量的氧气反应,生成的氧化物有两种能溶于稀硫酸,三种能溶于浓NaOH,氧化物的相对式量都大于26 |
⑵这四种元素含有铝元素吗? 。 |
| ③上述四中元素的单质的混合物,加入足量的盐 酸溶液,固体部分溶解,过滤,向滤液中加入过 量的烧碱溶液,最终溶液中有白色沉淀 |
⑶白色沉淀的化学式为。 |
| ④在W的最价氧化对应的水化合的含氧酸钠盐溶液中,加过量的盐酸能生成白色沉淀。 |
⑷生成白色沉淀的离子方程式为 。 |
| ⑤X与W同主族 |
⑸X的最高价氧化物的电子式为。 |
(II)已探明我国锰矿储量占世界第三位,但富矿仅占6.4%,每年尚需进口大量锰矿石。有人设计了把我国的贫菱锰矿(MnCO3含量较低)转化为高品位“菱锰矿砂”(MnCO3含量高)的绿色工艺。该工艺流程如下图所示: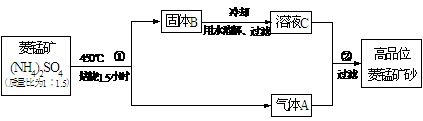
已知焙烧反应①的化学方程式:(NH4)2SO4+MnCO3 MnSO4+2NH3↑+CO2↑+H2O。
MnSO4+2NH3↑+CO2↑+H2O。
(1)写出反应②的离子方程式_______________________________________。
(2)上述工艺流程中,可以循环利用的物质有(NH4)2SO4、____________、__________。从物料平衡角度看,理论上生产过程中_________(填“需要”或者“不需要”)添加(NH4)2SO4。
能源问题日益成为制约世界经济发展的瓶颈,开发新能源,寻找经济发展的新动力,已受到许多国家的高度重视。二甲醚(CH3OCH3)可能成为未来替代柴油和液化气的洁净液体燃料,工业上在一定条件下以CO和H2为原料生产二甲醚的新工艺主要发生三个反应:
| 编号 |
热化学方程式 |
化学平衡常数 |
| ① |
CO(g)+2H2(g) CH3OH(g)△H1=-91kJ·mol-1 CH3OH(g)△H1=-91kJ·mol-1 |
K1 |
| ② |
2CH3OH(g) CH3OCH3(g)+H2O(g)△H2=-24kJ·mol-1 CH3OCH3(g)+H2O(g)△H2=-24kJ·mol-1 |
K2 |
| ③ |
CO(g)+H2O(g) CO2(g)+H2(g)△H3=-41kJ·mol-1 CO2(g)+H2(g)△H3=-41kJ·mol-1 |
K3 |
回答下列问题:
(1)新工艺的总反应为:3CO(g)+3H2(g) CH3OCH3(g)+CO2(g)△H
CH3OCH3(g)+CO2(g)△H
该反应△H=,化学平衡常数K=(用含K1、K2、K3的代数式表示)。
(2)下列措施中,能提高CH3OCH3产率的有。
A使用过量的CO B升高温度 C增大压强
D通入水蒸气 E.改用高效催化剂
(3)原工艺中反应①和反应②分别在不同的反应器中进行,无反应③发生。新工艺中反应③的发生提高了CH3OCH3的产率,原因是。
(4)为了寻找合适的反应温度,研究者进行了一系列试验,则每次试验应保持等因素不变。试验结果如下图,CO转化率随温度变化的原因是。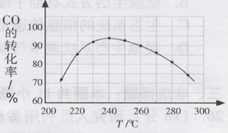
已知铅蓄电池的工作原理为Pb+PbO2+2H2SO4  2PbSO4+2H2O,现以铅蓄电池作电源,用惰性电极电解100 mL 4 mol·/L Cu(NO3)2溶液,一定时间后在阳极收集到标准状况下气体1.12 L。
2PbSO4+2H2O,现以铅蓄电池作电源,用惰性电极电解100 mL 4 mol·/L Cu(NO3)2溶液,一定时间后在阳极收集到标准状况下气体1.12 L。
(1)铅蓄电池中消耗的硫酸为mol;
(2)停止电解,向电解后的溶液中加入足量的铁粉,充分作用后溶液中的Fe2+的物质的量浓度为mol/L(设溶液的体积不变)。