下表是五种银盐的溶度积常数(25℃):
| 化学式 |
AgCl |
Ag2SO4 |
Ag2S |
AgBr |
AgI |
| 溶度积 |
1.8×10-10 |
1.4×10-5 |
6.3×10-50 |
7.7×10-13 |
8.51×10-16 |
下列说法错误的是( )
A.五种物质在常温下溶解度最大的是Ag2SO4
B.将氯化银溶解于水后,向其中加入Na2S,则可以生成黑色沉淀
C.对于AgCl、AgBr和AgI三种物质在常温下的溶解度随着氯、溴、碘的顺序增大
D.沉淀溶解平衡的建立是有条件的,外界条件改变时,平衡也会发生移动
下列叙述正确的是
| A.在共价化合物中一定存在共价键 |
| B.只存在共价键的物质一定是共价化合物 |
| C.含有共价键的化合物一定是共价化合物 |
| D.离子化合物中只含有离子键 |
能一次性鉴别(NH4)2SO4、NH4Cl 、NaCl 、Na2SO4四种无色溶液的试剂是
| A.Na OH | B.Ba(OH)2 |
| C.AgNO3 | D.BaCl2 |
已知质量数为A的某阴离子Rn-,核外有X个电子,则核内中子数为
| A.A-x | B.A-x-n | C.A-x+n | D.A+x-n |
核黄素又称为维生素B2,可促进发育和细胞再生,有利于增进视力,减轻眼睛疲劳。核黄素分子的结构为: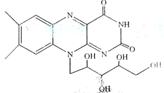
已知: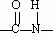 +H2O
+H2O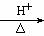
 +
+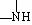
有关核黄素的下列说法中,不正确的是:
| A.该化合物的分子式为C17H22N4O6 |
| B.酸性条件下加热水解,有CO2生成 |
| C.酸性条件下加热水解,所得溶液加碱后有NH3生成 |
| D.能发生酯化反应 |
常温下,对下列各溶液的叙述不正确的是
| A.CH3COONa溶液中:c(OH-)=C(H+)+C(CH3COOH) |
| B.在pH=8的NaF溶液中,c(Na+)-c(F-)=9.9×10-7mol/L |
| C.pH=2的盐酸与pH=12的Ba(OH)2溶液等体积混合后,溶液中一定有C(H+)=C(OH-) |
| D.向0.1 mol/L氨水中加入少量NH4Cl固体,溶液中c(OH-)/c(NH3.H2O)增大 |