(1)在粗制CuSO4·5H2O晶体中常含有杂质Fe2+。在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质可采用的是________。A. KMnO4 B. H2O2 C. Cl2水 D. HNO3
然后再加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的________。A. NaOH B. NH3·H2O C. CuO D. Cu(OH)2
(2)甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常 温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10
温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10 -
- 5 mol·L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0 mol·L-1,则Cu(OH)2开始沉淀时溶液的pH为________,Fe3+完全沉淀时溶液的pH为________,通过计算确定上述方案________(填“可行”或“不可行”)。
5 mol·L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0 mol·L-1,则Cu(OH)2开始沉淀时溶液的pH为________,Fe3+完全沉淀时溶液的pH为________,通过计算确定上述方案________(填“可行”或“不可行”)。
磷单质及其化合物的有广泛应用。
(1)三聚磷酸可视为三个磷酸分子(磷酸结构式见图)之间脱去两个分子产物,其结构式为。三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为
(2)次磷酸钠(NaH2PO2)可用于化学镀镍。
①NaH2PO2中P元素的化合价为。
②化学镀镍的溶液中含有Ni2+和H2PO2-,在酸性等条件下发生下述反应:
(a)
(b)6H2PO2- +2H+ = 2P+4H2PO3-+3H2↑
某温度(T℃)时,测得0.01mol/LNaOH溶液的pH为11,则该温度下水的KW=____________。则该温度________(填“大于”、“小于”或“等于”)室温,其理由是_______________________________________________________________________。
此温度下,将pH=a的NaOH溶液VaL与pH=b的H2SO4溶液VbL混合,通过计算填写以下不同情况时两溶液的体积比:
(1)若所得混合溶液为中性,且a=12,b=2,则Va∶Vb=________。
(2)若所得混合溶液为中性,且a+b=12,则Va∶Vb=________。
(3)若所得混合溶液的pH=10,且a=12,b=2,则Va∶Vb=__________。
工业上制取纯净的CuCl2·2H2O的主要过程是:①将粗氧化铜(含少量Fe)溶解于稀盐酸中。加热、过滤,调节滤液的pH为3;②对①所得滤液按下列步骤进行操作: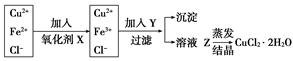
已知Cu2+、Fe2+在pH为4~5时不水解,而Fe3+却几乎完全水解而沉淀,请回答以下问题:
(1)X是________,其反应的离子方程式是___________________________________。
(2)Y物质应具备的条件是_________________,生产中Y可选______________________。
(3)溶液Z在蒸发结晶时应注意__________________________________________。
物质在水中可能存在电离平衡、盐的水解平衡等,它们都可看作化学平衡。请根据所学的知识回答:
(1)A为0.1mol•L-1的(NH4)2SO4溶液,在该溶液中各种离子的浓度由大到小顺序为。
(2)B为0.1 mol•L-1NaHCO3溶液,在NaHCO3溶液中存在的各种平衡体系为(分别用离子方程式表示):;实验测得NaHCO3溶液的pH>7,请分析NaHCO3溶液显碱性的原因:。
(3)C为FeCl3溶液,实验室中配制FeCl3溶液时通常需要向其中加入,目的是;将B和C溶液混合后,反应的离子方程式为。
某一元弱酸(用HA表示)在水中的电离方程式是:HA H++A-,回答下列问题:
H++A-,回答下列问题:
(1)向溶液中加入适量NaA固体,以上平衡将向________(填“正”、“逆”)反应方向移动,理由是______________________________________________________。
(2)若向溶液中加入适量NaCl溶液,以上平衡将向________(填“正”、“逆”、“不移动”)反应方向移动,溶液中c(A-)将________(填“增大”、“减小”或“不变”,下同),溶液中c(OH-)将________。