室温下,若溶液中由水电离产生的c(OH-)=1×10-14mol/L,满足此条 件的溶液中一定可以大量共存的离子组是( )
件的溶液中一定可以大量共存的离子组是( )
| A.Al3+、Na+、NO3-、Cl- | B.K+、Na+、Cl-、NO3- |
| C.K+、Na+、Cl-、AlO2- | D.K+、NH4+、SO42-、NO3- |
2005年3月29日,京沪高速公路上发生特大交通事故,一辆装 载近35吨液氯的槽车因爆胎与迎面大客车相撞大量液氯外泄,导致多人死伤。下列有关现场处置方法不正确的是
载近35吨液氯的槽车因爆胎与迎面大客车相撞大量液氯外泄,导致多人死伤。下列有关现场处置方法不正确的是
| A.槽罐吊入盛烧碱的临时水池中 | B.将人、畜迅速转移到地势较高的地方 |
| C.用毛巾浸透NaOH溶液捂住鼻子 | D.用毛巾浸透肥皂水或小苏打溶液捂住鼻子 |
如图所示,a、b、c均为石墨电极,d为碳钢电极,通电进行电解。假设在电解过程中产生的气体全部逸出,下列说法正确的是
| A.甲、乙两烧杯中溶液的pH均升高 |
B.当b极增重5.4g时,d极产生的 气体为2.24L(标准状况) 气体为2.24L(标准状况) |
| C.当电解一段时间后,将甲、乙两溶液混合,一定会生成沉淀 |
| D.乙烧杯中c的电极反应式为2Cl--2e-=Cl2↑ |
往一体积不变的密闭容器中充入H2和I2,发生反应H2(g) + I2(g) 2HI(g);
2HI(g);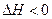 ,当达到平衡后,t0 时若保持混合气体总物质的量不变而改变某一反应条件,使容器内压强增大(如图所示),下列说法正确的是
,当达到平衡后,t0 时若保持混合气体总物质的量不变而改变某一反应条件,使容器内压强增大(如图所示),下列说法正确的是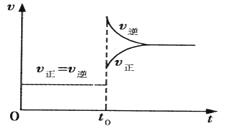
A.容器内气体颜色变深,平均相对分子质 量不变 量不变 |
| B.平衡不移动,混合气体密度增大 |
| C.H2转化率增大,HI平衡浓度减小 |
| D.t0 时减小体积或升高体系温度 |
有一无色溶液,可能含有K+、A13+、Mg2+、NH4+、Cl—、SO42—、HCO3—、MnO4—中的几种。为确定其成分,做如下实验:①取部分溶液,加入适量Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生。下列推断正确的
| A.肯定有A13+、Mg2+、NH4+、Cl— | B.肯定有Al3+、Mg2+、HCO3— |
| C.肯定有K+、HCO3—、MnO4— | D.肯定有A13+、Mg2+、SO42— |
在恒压密闭容器M(如图Ⅰ)和恒容密闭容器N(如图Ⅱ )中,分别加入a molA和a molB,起始时两容器体积均为V L,发生如下反应并达到化学平衡状态:2A(?)+ B(?)
)中,分别加入a molA和a molB,起始时两容器体积均为V L,发生如下反应并达到化学平衡状态:2A(?)+ B(?)
 xC(g);ΔH<0,平衡时M中A、B、C的物质的量之比为1∶3∶4。下列判断正确的是。
xC(g);ΔH<0,平衡时M中A、B、C的物质的量之比为1∶3∶4。下列判断正确的是。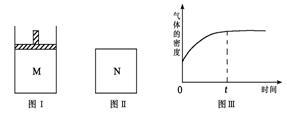
A.x=4
B.若N中气体的密度如图Ⅲ所示,则A、B都是气态
C.若A为气体,B为非气体,则平衡时M、N中C的物质的量相等
D.若A、B均为气体,平衡时M中A的转化率小于N中A的转化率