用NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A.0.5 mol锌粒与足量盐酸反应产生11.2 L H2 |
| B.标准状况下,11.2 L H2O所含分子数为0.5NA |
| C.0.5 mol•L﹣1的MgCl2溶液中含有Cl﹣个数为NA |
| D.25℃、101Pa时,16g O2和O3混合气体中含有的原子数为NA |
锌—空气电池可能成为未来的理想动力源,该电池的电解质溶液可以是酸性或碱性。在碱性溶液中该电池总反应可表示为:2Zn+4NaOH+O2=2Na2ZnO2 +2H2O。下列有关锌-空气电池说法正确的是
| A.碱性电解质溶液中正极反应式为:4OH-- 4e-= O2↑+2H2O |
| B.碱性或酸性电解质溶液中,该电池正极反应式相同 |
| C.该电池工作时,Na+移向负极 |
| D.每生成1 mol ZnO22-转移电子数为2NA |
在离子浓度都为0.1 mol/L的下列溶液中,加入(或通入)某物质后,发生反应先后顺序正确的是
| A.在含Fe3+、Cu2+、H+的溶液中加入锌粉:Cu2+、Fe3+、H+ |
| B.在含I-、SO32-、Br-的溶液中不断通入氯气:I-、Br-、SO32- |
| C.在含AlO2-、SO32-、OH-的溶液中逐滴加入硫酸氢钠溶液:OH-、AlO2-、SO32- |
| D.在含Fe3+、H+、NH4+的溶液中逐渐加入烧碱溶液:H+、NH4+、Fe3+ |
下列说法正确的是
| A.若以w1和w2分别表示浓度为amol·L-1和bmol·L-1氨水的质量分数,且知2a=b,则w2>2w1(氨水的密度比纯水的小) |
| B.7.8gNa2O2与CO2完全反应,转移0.2mol电子 |
| C.CO2、SO3、NO2和水反应均能生成酸,都属于酸性氧化物 |
| D.NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体 |
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系: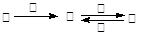 。下列有关物质的推断不正确的是
。下列有关物质的推断不正确的是
| A.若甲为焦炭,则丁可能是O2 |
| B.若甲为SO2,则丁可能是氨水 |
| C.若甲为Fe,则丁可能是盐酸 |
| D.若甲为NaOH溶液,则丁可能是CO2 |
在AlCl 和FeCl
和FeCl 混合溶液中,先加入过量的KI溶液,再加入足量的Na
混合溶液中,先加入过量的KI溶液,再加入足量的Na S溶液,所得 到的沉淀物是
S溶液,所得 到的沉淀物是
A.Fe(OH) 、Al(OH) 、Al(OH) |
B.Al(OH) 、I 、I |
C.Fe S S 、I 、I |
D.FeS、S、Al(OH) |