随着环保意识增强,清洁能源越来越受到人们关注。
(1)甲烷是一种理想的洁净燃料。已知:
CH4(g)+2O2(g)= CO2(g)+2H2O(g);△H= —802.3kJ·mol-1
H2O(1) =H2O(g),△H =+44.0kJ·mol-l
则4.8g甲烷气体完全按燃烧生成液态水,放出热量为 。
(2)利用甲烷与水反应制备氢气,因原料廉价,具有推广价值。
该反应为CH4(g)+H2O(g) CO(g)+3H2(g);△H=+206.lkJ·mol-l。
CO(g)+3H2(g);△H=+206.lkJ·mol-l。
①若800℃时,反应的化学平衡常数K=l.0,某时刻测得该温度下密闭容器中各物质的物质的量浓度如下表。
则此时正、逆反应速率的关系是 。(填标号)
| A.v(正)>v(逆) | B.v(正)<v(逆) |
| C.v(正)=v(逆) | D.无法判断 |
②为了探究温度、压强对上述化学反应速率的影响,某同学设计了以下三组对比实验(温度为360℃或480℃、压强为101 kPa或303 kPa,其余实验条件见下表)。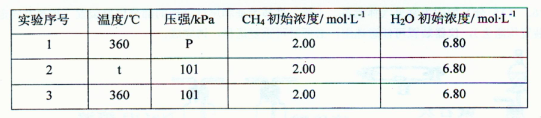
表中t= ,P= ;
设计实验2、3的目的是
实验l、2、3中反应的化学平衡常数的大小关系是 (用K1、K2、K3表示)。
已知:CO2(g) + 3H2(g)  CH3OH(g) + H2O(g) ΔH=-49.0 kJ•mol-1。一定条件下,向体积为1 L的密闭容器中充入1 mol CO2和3 mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如右图所示。下列叙述中,正确的是
CH3OH(g) + H2O(g) ΔH=-49.0 kJ•mol-1。一定条件下,向体积为1 L的密闭容器中充入1 mol CO2和3 mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如右图所示。下列叙述中,正确的是
A.升高温度能使 增大 增大 |
| B.反应达到平衡状态时,CO2的平衡转化率为75% |
| C.3 min时,用CO2的浓度表示的正反应速率等于用CH3OH的浓度表示的逆反应速率 |
| D.从反应开始到平衡,H2的平均反应速率υ(H2)=0.075 mol•L-1•min-1 |
已知某强酸性溶液中存在较多的Ba2+、NO3-,则溶液中还可能大量存在的离子组是
| A.K+、NH4+、HCO3- | B.Fe2+、Ca2+、Cl- |
| C.Cu2+、Mg2+、SO42- | D.Na+、Cu2+、Cl- |
下列叙述中,正确的是
A.1 mol 过氧化钠中阴离子所带的负电荷数为6.02×1023 |
B.14 g乙烯和丙烯的混合物中含有的碳原子的数目为6.02×1023 |
C.28 g C16O与28 g C18O中含有的质子数均为14×6.02×1023 |
D.标准状况下,22.4 L氯气与足量氢氧化钠溶液反应转移的电子数为2×6.02×1023 |
下列有关0.1 mol•L-1NaHCO3溶液中离子浓度的关系式,正确的是
| A.c(Na+) > c(HCO3-) > c(CO32-) > c(H+) > c(OH-) |
| B.c(Na+) > c(CO32-) > c(HCO3-) > c(OH-) > c(H+) |
| C.c(Na+) =c(HCO3-) + 2c(CO32-) + c(H2CO3) |
| D.c(Na+) + c(H+) =c(HCO3-) + 2c(CO32-) + c(OH-) |
短周期元素W、X、Y、Z在元素周期表中的位置如右图所示。下列说法中,正确的是
| A.W的最高价氧化物对应的水化物是强酸 |
| B.Y的原子半径在同周期主族元素中最大 |
| C.W的非金属性比Z的弱 |
| D.Z的气态氢化物的稳定性在同主族元素中最强 |