在pH都等于10的NaOH和CH3COONa两种溶液中,设由水电离产生的OH- 离子浓度分别为Amol/L与Bmol/L,则A和B关系为
A.A>B B.A=10-6 B C.B=10-6 A D.A="B "
为证明稀硝酸与铜反应产物中气体为NO,设计如图实验(实验过程中活塞2为打开状态),下列说法中不正确的是 ( )。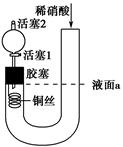
| A.关闭活塞1,加入稀硝酸至液面a处 |
| B.在装置左侧稍加热可以加快稀硝酸与铜的反应速率 |
| C.通过关闭或开启活塞1可以控制反应的进行 |
| D.反应开始后,胶塞下方有无色气体生成,还不能证明该气体为NO |
下列实验操作正确的是 ( )。
| A.中和滴定实验时,用待测液润洗锥形瓶 |
| B.盛放NaOH溶液时,使用带玻璃塞的磨口瓶 |
| C.用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 |
| D.NaCl溶液蒸发结晶时,蒸发皿中有晶体析出并剩余少量液体即停止加热 |
在实验室中进行下列实验探究,其中的实验用品均能用到且正确的是( )。
| 选项 |
实验探究内容 |
实验用品 |
| A |
铜丝在氯气中燃烧 |
坩埚钳、燃烧匙、氯气、铜丝 |
| B |
铝热反应 |
铁架台、大蒸发皿、普通漏斗、铝粉、Fe2O3 |
| C |
实验室制备氨气 |
试管、集气瓶、酒精灯、NH4Cl、Ca(OH)2 |
| D |
用KMnO4晶体配制500 mL 0.1 mol·L-1 KMnO4溶液 |
容量瓶、烧杯、玻璃棒、酸式滴定管、KMnO4 |
下列实验装置设计正确,且能达到目的的是(双选) ( )。
| A.实验Ⅰ:检查装置的气密性 |
| B.实验Ⅱ:测定未知盐酸的浓度 |
| C.实验Ⅲ:制取并观察Fe(OH)2沉淀 |
| D.实验Ⅳ:配制一定物质的量浓度的稀硫酸溶液 |
“封管实验”具有简易、方便、节约、绿色等优点,观察下列四个“封管实验”(夹持装置未画出),判断下列说法正确的是
( )。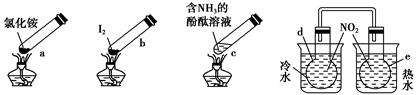
| A.加热时,a上部聚集了固体NH4Cl,说明NH4Cl的热稳定性比较好 |
| B.加热时,发现b中I2变为紫色蒸气,在上部又聚集为紫黑色的固体 |
| C.加热时,c中溶液红色变深,冷却后又变浅 |
| D.e内气体颜色变浅,d内气体颜色加深 |