某学生为测定未知浓度的硫酸溶液,实验如下:以0.14mol/L的NaOH溶液滴定上述稀H2SO420.00mL,滴定终止时消耗NaOH溶液16.00mL。
(1)该学生用标准0.14 mol/L NaOH溶液滴定硫酸的实验操作如下:
A.用酸式滴定管取稀H2SO4 20.00 mL,注入锥形瓶中,加入指示剂。
B.用待测定的溶液润洗酸式滴定管。
C.用蒸馏水洗干净滴定管。
D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2~3 cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下。
E.检查滴定管是否漏水。
F.另取锥形瓶,再重复操作一次。
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。
①滴定操作的正确顺序是(用序号填写):E—( )—D—( )— ( )—( )—F 。
②该滴定操作中应选用的指示剂是: 。
③在G操作中如何确定终点?  。
。
(2)用标准的NaOH滴定未知浓度的盐酸 ,选用酚酞为指示剂,造成测定结果偏高的原因可能是_________。
,选用酚酞为指示剂,造成测定结果偏高的原因可能是_________。
A.配制标准溶液的氢氧化钠中混有NaCl杂质
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
E.未用标准液润洗碱式滴定管
F.开始实验时碱式滴定管尖嘴部分有气泡,在滴定过程中气泡消失,则测得盐酸浓度
(3)计算待测硫酸 溶液的物质的量浓度 mol/L(计算结果保留二位有效数字)
溶液的物质的量浓度 mol/L(计算结果保留二位有效数字)
某学生应用下图所示的装置来研究物质的性质,其中气体X的主要成分是氯气,杂质是空气和水蒸气。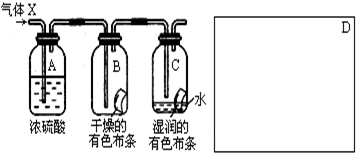
回答下列问题:
(1)该项研究(实验)的主要目的是。
(2)浓H2SO4的作用是,
与研究目的直接相关的实验现象是______________________________________。
(3)该实验装置设计上存在的缺陷为 _________________ ,
请在上图的D处画出能克服该缺陷的装置。
(14分)高锰酸钾俗称PP粉,为强氧化剂,遇到有机物就放出活性氧。这种氧有杀灭细菌的作用,且杀菌能力极强。某学生欲在实验室配制1 L 0.06 mol/L KMnO4稀溶液,用来清洗伤口。
(1)实验过程中需用托盘天平称取KMnO4晶体的质量为__________g。
(2)其操作步骤如下图所示,则右图所示操作应在下图中__________(填选项字母)之间。
A.②与③ B.①与② C.④与⑤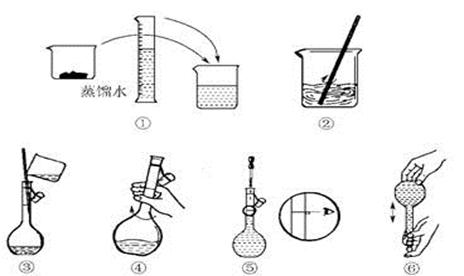
(3) 配制过程中需要用到的仪器有:托盘天平、药匙、烧杯、、、
(4)若该同学在配制溶液时,进行了如下操作,其中使所配溶液浓度偏低的操作
有_______________(填选项字母)。
A.称量KMnO4晶体时,指针偏向右边
B.将KMnO4晶体放在烧杯中溶解,冷却后,转移至含有少量蒸馏水的容量瓶中
C.定容时,仰视刻度线
D.振荡摇匀后,发现溶液液面低于刻度线,再滴加少量蒸馏水至刻度线处
盐酸、硝酸都是用途相当广泛的两种酸。
(1)瑞典科家舍勒在研究软锰矿(主要成份为MnO2)时,将浓盐酸与软锰矿混合加热,产生了一种有刺激性气味的有色气体。写出该反应的化学方程式,并标出电子转移方向和数目: 。
(2)某校合作学习探究小组学习科学家探究精神对氯气性质进行了探究,设计了以下一些实验。
| 实验内容 |
实验现象 |
|
| A |
收集一集气瓶气体,观察颜色,然后向瓶内倒入约占瓶容积1/5的蒸馏水,充分振荡。 |
蒸馏水呈浅黄绿色,瓶内气体仍呈黄绿色。 |
| B |
取出瓶内部分溶液,滴入紫色石蕊试液中直至过量。 |
紫色石蕊试液先变红色,后红色褪色。 |
| C |
取出瓶内剩下的部分溶液,滴入硝酸银溶液中。 |
产生大量白色沉淀 |
| D |
最后向瓶内倒入少量浓氢氧化钠溶液,振荡。 |
瓶内黄绿色气体立即消失。 |
①能说明氯气与水发生化学反应的实验是(填实验序号)
②写出实验D中所发生反应的离子方程式。
(3)该校另一合作学习探究小组用下列左图所示装置对铜与硝酸反应进行探究。
①甲同学观察到试管中的气体由无色变成了红棕色,由此认为试管里的硝酸是浓硝酸,你认为他的看法正确吗?。为什么?。
甲同学还能观察到的现象有。
②乙同学向反应完成后的溶液里滴加氢氧化钠溶液,产生的沉淀(m/g)和加入溶液的体积(V/mL)的关系如上右图所示。请写出O-A段反应的离子方程式 。
为研究某铁质材料与浓硫酸反应生成气体的成分,某学习小组进行了以下探究活动:
(1)称取铁钉5.6g放入20mL足量浓硫酸中,加热,理论上收集到气体SO2L(标况)。将所得气体全部通入足量溴水中,然后加入足量BaCl2溶液,经适当操作后得干燥固体23.3g。由此推知实际生成气体SO2的体积为L(标况)。
(2)分析上述实验中SO2体积的结果,有同学认为所得气体中除含有 SO2外,还可能含有H2和Q气体。为此设计了下
SO2外,还可能含有H2和Q气体。为此设计了下 列探究实验装置(图中夹持仪器省略)。
列探究实验装置(图中夹持仪器省略)。
①装置A中试剂的作用是
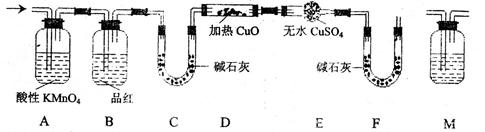
②认为气体中还含有的Q气体是
③为确认Q的存在,需在装置中添加M于,
a.A之前 b.AB之间 c.BC之间 d.CD之间
M中的试剂是
④如果气体中含有H2,预计实验现象应是
试回答下列问题:(1)下 列实验中所选用的仪器或操作以及结论不合理的是
列实验中所选用的仪器或操作以及结论不合理的是
A.用托盘天平称量11.7g氯化钠晶体
B.用碱式滴定管量取20.00mL Na2CO3溶液
C.加热NH4Cl晶体时,用湿润红色石蕊试纸靠近试管口,检验NH3的生成
D.测定溶液的pH时,用洁净、干燥的玻璃棒蘸取溶液,滴在用蒸馏水湿润过的pH试纸上与标准比色卡比较
E.仅用蒸馏水和pH试纸,就可以鉴别pH相等的H2SO4和CH3COOH溶液
(2)海洋植物海带中含有大量的碘 元素,碘元素以碘离子的形式存在。实验室里从海带中提取碘的流程如下图:
元素,碘元素以碘离子的形式存在。实验室里从海带中提取碘的流程如下图: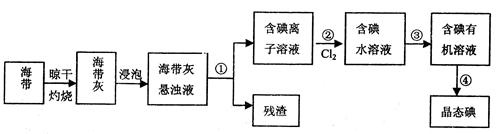
I.指出提取碘的过程中有关的实验操作名称:①,③
II.提取碘的过程中,可供选择的有机试剂是(填序号)
A.甲苯、酒精 B.四氯化碳、苯
C.汽油、乙酸 D.汽油、甘油
III.为使碘水溶液转化为碘的有机溶液,实验室有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品,尚缺少的玻璃仪器有