下列离子方程式书写正确的是
| A.在FeCl3溶液中加入铁粉:Fe3++Fe |
| B.锌与18.4mol·L--1的H2SO4溶液反应:Zn+2H+ |
| C.用NaOH溶液吸收氯气:C12+2OH-=Cl-+ClO-+H2O |
| D.稀H2SO4与Ba(OH)2溶液反应:Ba2++2OH-+SO42-+2H+ |
下列叙述中正确的是
| A.原子及其离子的核外电子层数等于该元素所在周期数 |
| B.稀有气体元素原子的最外层电子数都是8 |
| C.元素周期表从ⅢB到ⅡB 10个纵行的元素都是金属元素 |
| D.短周期元素中,若两种元素的原子序数相差8,则它们的周期数一定相差1 |
下列有关实验操作、现象和解释或结论都正确的是
| 选项 |
实验操作 |
现象 |
解释或结论 |
| A |
过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液 |
溶液呈红色 |
稀HNO3将Fe氧化为Fe3+ |
| B |
5mL4%的过氧化氢溶液中加入少量MnO2粉末 |
迅速产生大量气泡 |
催化剂能显著地增大化学反应速率 |
| C |
Al箔插入稀HNO3中 |
无现象 |
Al箔表面被HNO3氧化,形成致密的氧化膜 |
| D |
用石墨棒做电极,电解氯化铜溶液 |
产生使湿润的淀粉碘化钾试纸变蓝的黄绿色气体 |
该气体为Cl2,放出该气体的电极为电解池的阳极 |
以下说法正确的是
| A.C60与金刚石互为同素异形体,它们都属于原子晶体 |
| B.干冰升华既克服了分子间作用力,也破坏了共价键 |
| C.金属元素和非金属元素形成的化合物在熔融状态下一定能导电 |
| D.NaCl晶体溶于水破坏了Na+和Cl-之间的离子键 |
对于以下反应:A(s)+3B(g)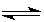 2C(g)+D(g),在一定温度、体积固定的密闭容器中进行,下列叙述中能说明上述反应达到平衡状态的是
2C(g)+D(g),在一定温度、体积固定的密闭容器中进行,下列叙述中能说明上述反应达到平衡状态的是
A.混合气体的密度不随时间变化而变化
B.单位时间内每消耗3 mol B,同时生成2 mol C
C.D的物质的量分数在混合气体中保持不变
D.B、C、D的分子个数之比为3∶2∶1
a、b、c、d、e是同周期的五种元素,a和b的最高价氧化物的水化物显碱性,且将a、b相连浸入稀硫酸中时,a溶解而b表面有气泡产生;c和d的气态氢化物的还原性d>c,五种元素的原子,得失电子后所形成的简单离子中,e的离子半径最小,则它们的原子序数由小到大的顺序是
| A.b、a、e、d、c | B.e、d、a、b、c | C.a、b、e、d、c | D.a、b、d、c、e |