在“十二五”期间,江苏省将大力实施“清水蓝天”工程。下列不利于“清水蓝天”工程实施的是
| A.加大稀土资源的开采和出口,保证经济快速发展 |
| B.加强城市生活污水脱氮除磷处理,遏制水体富营养化 |
| C.积极推广太阳能、风能、地热能及水能等的使用,减少化石燃料的使用 |
| D.大力实施矿物燃料“脱硫、脱硝技术”,减少硫的氧化物和氮的氧化物污染 |
下列过程中,共价键被破坏的是()
| A.碘升华 | B.溴蒸气被木炭吸附 |
| C.酒精溶于水 | D.HCl气体溶于水 |
某烃的结构简式是 ,它不可能具有的性质是
,它不可能具有的性质是
| A.它能使溴水褪色,也能使酸性KMnO4溶液褪色 |
| B.易溶于水,也易溶于有机溶剂 |
C.能发生加聚反应,生成物可用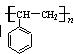 表示 表示 |
| D.该烃能与H2一定条件下反应 |
短周期主族元素A、B、C、D,原子序数依次增大。A、C的原子序数的差为8,A、B、C三种元素原子的最外层电子数之和为15,B原子最外层电子数等于A原子最外层电子数的一半。下列叙述正确的是
A.原子半径:A<B<C<D B.非金属性:A>C
C.最高价氧化物对应水化物的酸性:D>C D.单质B常温下能溶于浓硝酸
减少酸雨产生的途径可采取下列中的哪些措施:①少用煤作燃料②把工厂烟囱造高③燃料脱硫④飞机、汽车等交通工具采用清洁燃料,如天然气、甲醇等⑤开发新能源
| A.①②③④ | B.②③④⑤ | C.①②③⑤ | D.①③④⑤ |
下面实验操作可以实现实验目的的是
| A.鸡蛋白溶液中,加入浓的硫酸铵溶液有沉淀析出,加入水后沉淀不溶解 |
| B.将SO2通入酸性KMnO4溶液中,溶液褪色,证明SO2具有漂白性 |
| C.取样灼烧,可以鉴别某白色纺织品是棉织品还是羊毛制品 |
| D.取少量蔗糖溶液加稀硫酸,水浴加热几分钟后,再加入新制的氢氧化铜悬浊液并且加热,观察现象,判断蔗糖水解的产物中是否含有葡萄糖 |