(6分)将3.2 g Cu与足量的浓硫酸在加热条件下充分反应。
(1)其中被还原的硫酸的物质的量为 。
(2)把反应后的溶液稀释至500 mL,取出50 mL,向其中加入足量的BaCl2溶液,得到沉淀20.97 g,则稀释后所得溶液中SO42-的物质的量浓度为 。
(3)若浓硫酸中含溶质为b mol,投入足量的铜片并加热,充分反应后,被还原的硫酸的物质的量n (H2SO4) 0.5 b mol(填“>”、“<”或“=”)。
某反应,在不同反应时间各物质的量变化情况如图所示。则该反应的反应物(用A、B、C的字母填写)化学方程式为;
若反应在5L的密闭容器中进行,反应进行到2min时用A表示的化学反应速率为。2分钟后A、B、C各物质的量不再随时间的变化而变化,说明在这个条件下,反应已达到了状态。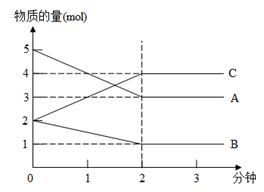
在一定温度下,将0.20 mol 的四氧化二氮气体充入1L的固定的密闭容器中,每隔一段时间对该容器内的物质进行一次分析,得到如下数据:
 时间 (s)浓度 mol·L-1 |
0 |
20 |
40 |
60 |
80 |
100 |
| C(N2O4) |
0.20 |
C1 |
0.10 |
C3 |
C4 |
C5 |
| C(NO2) |
0.00 |
0.12 |
C2 |
0.22 |
0.22 |
0.22 |
根据表格提供数据,请回答下列各小题:
⑴该反应的化学方程式为:
表示C2C3C4 (填 < , > 或 = )
⑵ 20S时,四氧化二氮的浓度C1=
在0~20 S内四氧化二氮的平均反应速度为
在容积为5L的密闭容器中,通入5 mol N2和8 mol H2,在一定条件下反应生成NH3,当反应进行到2 min时,测得容器内有4 mol NH3。则:
 (1)2 min时,容器内n(N2)==,c(H2)==。
(1)2 min时,容器内n(N2)==,c(H2)==。
(2)2 min内,以N2表示的平均反应速率v(N2)==。
 (3)2 min时,容器内气体的总物质的量与反应前容器内气体的总物质的量之比为:
(3)2 min时,容器内气体的总物质的量与反应前容器内气体的总物质的量之比为:
已知反应:FeO(s)+CO(g) = Fe(s)+CO2(g) 的Kc=0.5(1273K)。若起始浓度c(CO)=0.05 mol/L,c(CO2)=0.01 mol·L-1,请回答:
(1)判断化学反应进行的方向并计算反应物、生成物的平衡浓度。
(2)CO的转化率是多少?
(3)增加FeO的量,对平衡有无影响?
将锌片和铜片用导线相连浸入稀硫酸中组成原电池,两电极间连接一个电流计,装置如图: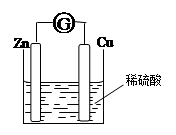
(1) 锌片上发生的电极反应:;
铜片上发生的电极反应:;
(2)若该电池中两电极的总质量为60g,工作一段时间后,
取出锌片和铜片洗净干燥后称重,总质量为47g,试计算产生标准状况
氢气的体积为多少L?