用化学用语填空:
(1)2个铵根离子 ;
(2)硫酸根离子 ;
(3)写出氯化铁的化学式并标出该化合物中铁元素的化合价 ;
参观溶洞景观。
【资料卡片】溶洞都分布在石灰岩(主要成分为碳酸钙)组成的山体中,石灰岩遇到溶有二氧化碳的水时,会生成溶解性较大的碳酸氢钙〔Ca(HCO3)2〕。溶有碳酸氢钙的水遇热或当压强突然变小时,溶解在水里的碳酸氢钙就会分解,重新生成碳酸钙沉积下来,同时放出二氧化碳。天长日久就会形成形态各异的石笋和钟乳石。
(1)石灰岩属于 (填“混合物”或“纯净物”)。
(2)形成碳酸氢钙的原因是 (用化学方程式表示)。
到达景区。
(1)景区繁花似锦、鸟语花香。从分子的角度解释“花香四溢”的原因 。
(2)玫瑰花香中含有香茅醇、橙花醇和丁香油酚等物质。其中丁香油酚(C10H12O2)的相对分子质量是 。
(3)为了维护景区优美的环境,不能随便丢弃垃圾。下列垃圾应投入可回收垃圾箱的是(填字母序号)。
A.易拉罐 B.果皮 C.矿泉水瓶
乘坐汽车。
(1)汽车电路中,常用铜做导线,这利用了铜的延展性和 。
(2)车体的主要材料为钢(铁的一种合金),工业上用赤铁矿炼铁的化学方程式是 。
出发前购买食品。
(1)食品包装中充入的氮气可以防腐,这利用了氮气的性质是 。
(2)雪碧属于“碳酸”饮料。二氧化碳与水反应的化学方程式是 。
(3)右图是某品牌矿泉水的部分标签内容,其中钠离子的符号是 。
根据下列装置图,回答问题: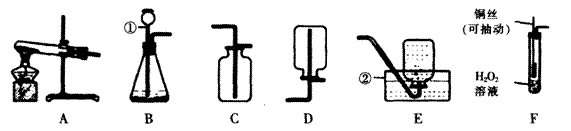
(1)写出仪器名称:①_________;②_________。
(2)实验室制取氢气,应选择发生装置是______________(填编号);若用排空气法收集,应选择收集装置是_________(填编号)。
(3)实验室用过氧化氢制取氧气的化学方程式:_____________。若用装置E收集氧气,实验结束时,移出导管,再_____________,取出集气瓶后,瓶口______________
(填“向上”或“向下”)放置于桌面。
(4)实验改进:查阅资料发现,氧化铜可用作过氧化氢分解制氧气的催化剂。现将一根绕成螺旋状的、表面已被氧化的铜丝组装成装置F(如图所示,已略去夹持装置)。
①铜丝绕成螺旋状的作用是_________(填编号);
a.制取更多氧气 b.增大接触面 c.没有影响
②与装置B比较,改进后装置F的优点是_____________。