短周期主族元素A、B、C、D、E、F的原子序数依次增大,它们的原子核外电子层数之和为13。已知B元素形成的化合物种类最多,D元素原子最外层电子数是次外层电子数的3倍,元素E的原子半径在同周期中最大,F元素原子最外层电子数等于其电子层数。
(1)C元素在元素周期表中的位置是_____________________,B的单质与C的最高价氧化物对应水化物的浓溶液发生反应的化学方程式是_________________
(2)由A、B、D、E四种元素形成的化合物中所含的化学键类型是_______________
(3)写出E2D2与A2D反应的离子方程式_____________________________________。
(4)实验室配制100mL0.2mol·L—1由A、D、E形成化合物的溶液,需要用到的玻璃仪器除烧杯、量筒外还有_________________________;如果定容时仰视刻度线,则所配制溶液浓度______________0.2mol·L—1(埴“>”、“<”或“=”)。将F的单质溶于上述配制的溶液中所发生反应的离子方程式是___________________________________
(14分)以下是一些物质的熔沸点数据(常压):
| 钾 |
钠 |
Na2CO3 |
金刚石 |
石墨 |
|
| 熔点(℃) |
63.65 |
97.8 |
851 |
3550 |
3850 |
| 沸点(℃) |
774 |
882.9 |
1850(分解产生CO2) |
--- |
4250 |
金属钠和CO2在常压、890℃发生如下反应:
4Na(g)+3CO2(g) 2Na2CO3(1)+C(s,金刚石);△H=-1080.9kJ/mol
2Na2CO3(1)+C(s,金刚石);△H=-1080.9kJ/mol
(1)上述反应的平衡常数表达式为;若4v正(Na)=3v逆(CO2),反应是否达到平衡(选填“是”或“否”)。
(2)若反应在10L密闭容器、常压下进行,温度由890℃升高到1860℃,若反应时间为10min,金属钠的物质的量减少了0.2mol,则10min里CO2的平均反应速率为。
(3)高压下有利于金刚石的制备,理由。
(4)由CO2(g)+4Na(g)=2Na2O(s)+C(s,金刚石) △H=-357.5kJ/mol;则Na2O固体与C(金刚石)反应得到Na(g)和液态Na2CO3(1)的热化学方程式:。
(5)下图开关K接M时,石墨作极,电极反应式为。当K接N一段时间后,测得有0.3mol电子转移,作出y随x变化的图象【x—代表n(H2O)消耗,y—代表n[Al(OH)3],反应物足量,标明有关数据】
(18分)已知有机物F和高分子N的合成路线如图所示:

(1)2 mol F生成l mol G。Q只含碳、氢、氧三种元素,且其碳、氢、氧元素质量比为9:1:6,经测定Q的相对分子质量是128。1 mol Q可与l mol Br2加成,并能与l molNaHCO3恰好完全反应,且分子中无支链。Q的分子式是。
(2)A所含官能团的名称是、;A→B的反应类型是;
(3)写出C与银氨溶液反应的化学方程式:;
(4)G的结构简式是;Q的反式结构简式是。
(5)下列说法正确的是 。
a.D催化加氢的产物与F互为同分异构体
b.F能发生氧化反应、取代反应、加成反应
c.高分子N的每条分子链中含有(n-1)个酯基
(6)写出满足下列条件H的一种同分异构体的结构简式
①能与NaHCO3反应 ②能发生银镜反应 ③核磁共振氢谱有4个吸收蜂
(7)写出H N的化学方程式:。
N的化学方程式:。
(14分)A、B、C、D、E、F六种短周期元素,其原子序数依次增大,其中B与C同周期,D与E和F同周期,A与D同主族,C与F同主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期原子半径最大的主族元素。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。
请回答下列问题。
(1)元素D在周期表中的位置。
(2)C、D、F三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示)。
(3)若E是非金属元素,其单质在电子工业中有重要应用,请写出其氧化物溶于强碱溶液的离子方程式:。
(4)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出反应的化学方程式:。冶炼金属E时,用石墨做电极。E在(填“阴”或“阳”) 极得到,电解过程中,阳极石墨需要不断补充,结合电极反应说明其原因是。
(5)由A、B、C三种元素以原子个数比4:2:3形成化合物X,X中所含化学键类型有。土壤中含有X中的阳离子在硝化细菌的催化作用下被氧气氧化为其阴离子,写出其离子方程式:。
(9分)某有机化合物A含碳76.6%、含氢6.4%,A的相对分子质量约是甲烷的5.9倍。在常温下,该有机物的稀溶液可与浓溴水反应生成白色沉淀,1molA恰好跟3molBr2反应。
(1)求A的分子式 。
(2)写出A的稀溶液中滴加浓溴水的化学方程式。
(3)写出A与碳酸钠、碳酸氢钠溶液可能发生的反应的离子方程式。
(12分)乙烯是重要的化工原料,可以合成很多有机物。以下转化关系中A-J均为有机化合物,H为有芳香气味的液体,F的分子式为C2H2O2,I分子中有一个六原子环状结构。部分反应条件和生成物已略去。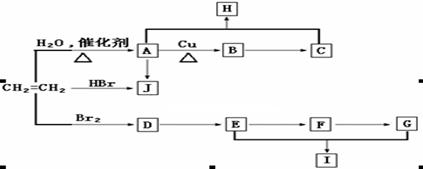
完成下列问题:
(1)写出A生成B的化学方程式:
(2)写出A生成J的化学方程式:
(3)写出D生成E的化学方程式:
(4)写出E和G生成I的化学方程式: