按官能团分类,下列说法正确的是
A.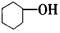 属于芳香化合物 属于芳香化合物 |
B.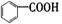 属于羧酸 属于羧酸 |
C. 属于醛类 属于醛类 |
D.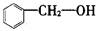 属于酚类 属于酚类 |
下列实验操作或原理不正确的是
| A.读取滴定管内液体体积时,俯视读数导致读数偏小 |
| B.分液操作时,分液漏斗中的下层液体从下口放出,上层液体从上口倒出 |
| C.纸层析法中的展开剂之所以能够展开的主要原理是毛细现象 |
| D.进行焰色反应时,必须用稀硫酸洗涤并灼烧铂丝,然后再进行实验 |
下列溶液中微粒的物质的量浓度关系正确的是
| A.25℃时,pH=7的NH4Cl与NH3•H2O混合溶液:c(H+)=c(OH-)=c(NH4+)=c(Cl-) |
| B.0.1mol/LNa2S溶液:c(OH-)=c(H+)+c(HS-)+c(H2S) |
| C.25℃时,pH=2的CH3COOH与pH=12的NaOH等体积混合: c(CH3COO-)+c(H+)<c(Na+)+c(OH-) |
| D.0.1mol/LNa2CO3溶液:2c(CO32-)+2c(HCO-)+2c(H2CO3)=c(Na+) |
如图为周期表中短周期的一部分,若X原子最外层电子数比次外层电子数少3,则下列说 法正确的是
| R |
||
| X |
Y |
Z |
A.X的氢化物比R的氢化物稳定
B.原子半径大小顺序是Z>Y>X
C.Y、R形成的化合物YR2能使KMnO4溶液褪色
D.X、Z可形成化合物XZ5,分子中各原子均满足最外层8电子结构
燃烧2mol某有机物,可以收集到标准状况下89.6L的CO2和6mol的H2O,试推断该有机物的分子式可能是
| A.C2H4 | B.C2H6O | C.C2H4O2 | D.C3H6O |
向下列溶液滴加稀硫酸,生成白色沉淀,继续滴加稀硫酸,沉淀又溶解的是
| A.Na2SiO3 | B.BaCl2 | C.CaCl2 | D.NaAlO2 |