由短周期元素组成的甲、乙、丙、丁四种物质分别含有两种或两种以上元素,它们分子中质子总数均与氩原子的质子数相同,已知甲是气态氢化物,在水中分步电离出两种阴离子。下列推断合理的是()
| A.某钠盐溶液含甲电离出的阴离子,则该溶液显碱性,只能与酸反应 |
| B.乙与氧气的摩尔质量相同,则乙一定含有极性键和非极性键 |
| C.丙中含有第2周期IV A族的元素,则丙一定是甲烷的同系物 |
| D.丁和甲含有相同元素,且该元素在二者中的百分含量相同,则丁中一定含有-l价的元素 |
近年来,加“碘”食盐较多使用了碘酸钾,KIO3可通过电解KI溶液(石墨和铁为电极)制备,反应式为KI+3H2O KIO3+3H2↑,下列说法正确的是()
KIO3+3H2↑,下列说法正确的是()
| A.电解时,石墨做阴极,铁做阳极 |
| B.电解时,在阳极产生氢气 |
| C.电解后得KIO3产品的步骤有:过滤→浓缩→结晶→灼烧 |
| D.电解中,每转移0.6 mol电子,理论可得0.1 mol无水KIO3晶体 |
如图中x、y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色无臭气体放出。符合这一情况的是()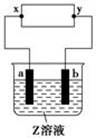
| a极板 |
b极板 |
x电极 |
Z溶液 |
|
| A |
锌 |
石墨 |
负极 |
CuSO4 |
| B |
石墨 |
石墨 |
负极 |
NaOH |
| C |
银 |
铁 |
正极 |
AgNO3 |
| D |
铜 |
石墨 |
负极 |
CuCl2 |
甲、乙、丙三个烧杯中分别装有稀硫酸、氯化铜溶液、饱和食盐水,把用导线连接的锌片和铜片插入甲,把分别与直流电源正、负极相连的C1、C2插入乙,把分别与直流电源正、负极相连的C3、铁片插入丙。则下列叙述正确的是()
| A.甲、丙中是化学能转变为电能,乙中是电能转变为化学能 |
| B.C1、C2分别是阳极、阴极,锌片、铁片上都发生氧化反应 |
| C.C1和C3放出的气体相同,铜片和铁片放出的气体也相同 |
| D.甲、乙中溶液的pH逐渐升高,丙中溶液的pH逐渐减小 |
铁镍蓄电池又称爱迪生电池,放电时的总反应为:Fe+Ni2O3+3H2O=Fe(OH)2+2Ni(OH)2。下列有关该电池的说法不正确的是()
| A.电池的电解液为碱性溶液,正极为Ni2O3、负极为Fe |
| B.电池放电时,负极反应为Fe+2OH--2e-===Fe(OH)2 |
| C.电池充电过程中,阴极附近溶液的pH降低 |
| D.电池充电时,阳极反应为2Ni(OH)2+2OH--2e-=Ni2O3+3H2O |
往含0.2 mol NaOH和0.1 mol Ba(OH)2的溶液中持续稳慢地通入CO2气体,使CO2气体充分参加反应,当通入气体为6.72 L(S.T.P)时立即停止,则这一过程中,溶液中离子的物质的量和通入CO2气体的体积关系正确的图像是(气体的溶解忽略不计) ( )



A.B.C.D.