a、b、c、d是四种短周期元素。a、b、d同周期,c、d同主族。a的原子结构示意图为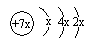 ,b与c形成化合物的电子式为
,b与c形成化合物的电子式为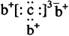 。下列比较中正确的是
。下列比较中正确的是
| A.原子半径:a>c>d>b | B.电负性a>b>d>c |
| C.原子序数:a>d>b>c | D.最高价含氧酸的酸性c>d>a |
下列混合物的物质的量一定时,组内各物质按任意比混合,完全燃烧时耗O2的量不变的是
| A.甲烷、甲醇、甲醛 |
| B.乙炔、苯、1,3-丁二烯 |
| C.丙烯、2-丁烯、环已烷 |
| D.乙醇、乙烯、丙烯酸(CH2=CH-COOH) |
某饱和一元醛和酮(RCOR')的混和物共0.5mol,质量为26.2g,该混和物与足量银氨溶液作
用,最多析出43.2g银。则混和物中的醛可能是 ( )
| A.乙醛 | B.丁醛 | C.戊醛 | D.已醛 |
已知乙烯醇(CH2==CHOH)不稳定,可自动转化为乙醛;二元醇可脱水生成环状化合物。现有1 mol乙二醇在一定条件下脱去1 mol水,所得产物的结构简式有下列几种,其中不可能的是 ( )
| A.只有① | B.只有①④ | C.只有①⑤ | D.有①④⑤ |
下图表示取1 mol乙烯雌酚进行的四个实验,下列对实验数据的预测与实际情况吻合的是( )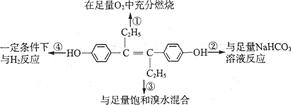
| A.①中生成7 mol H2O | B.②中生成2 mol CO2 |
| C.③中最多消耗3 mo1 Br2 | D.④中最多消耗7 mol H2 |
经测定,由C3H7OH和C6H12组成的混合物中氧的质量分数为8%,则此混合物中氢的质量
分数为 ()
| A.78% | B.22% | C.14% | D.13% |