下列有关物质的性质和该性质的应用均正确的是( )
| A.常温下浓硫酸能使铝发生钝化,可在常温下用铝制容器贮藏贮运浓硫酸 |
| B.二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
| C.明矾可用以水的消毒杀菌 |
| D.铜的金属活泼性比铁的差,可在海轮外壳上装若干铜块以减缓其腐蚀 |
世博会上澳大利亚馆的外墙采用的是特殊的耐风化钢覆层材料,外墙的颜色每天都在发生着变化,它会随空气中太阳、风雨、湿度的影响,逐渐结出一层锈斑,从橙色到赭红色的转变,看上去外观的生锈程度在增加,运用了钢材生锈原理。下列有关钢材生锈的说法正确的是 
| A.红色铁锈的主要成分是Fe(OH)3 |
| B.钢材在空气中的变化只有氧化还原反应 |
| C.钢材在空气中的腐蚀主要为电化腐蚀,其负极的反应为:Fe-3e-=Fe3+ |
| D.空气中太阳、风雨、湿度对钢材的腐蚀有影响 |
今有如下三个热化学方程式:
H2(g)+ 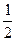 O2(g)="=" H2O(g) ΔΗ="a" kJ·mol-1
O2(g)="=" H2O(g) ΔΗ="a" kJ·mol-1
H2(g)+ 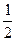 O2(g)="=" H2O(l) ΔΗ="b" kJ·mol-1
O2(g)="=" H2O(l) ΔΗ="b" kJ·mol-1
2H2(g)+O2(g)="=" 2H2O(l) ΔΗ="c" kJ·mol-1
关于它们的下列表述正确的是
A.它们都是吸热反应 B.a、b和c均为正值
C .a=b D.2b=c
.a=b D.2b=c
一定温度下,在密闭容器中发生反应:A(g)+3B(g)  2C(g)达到平衡的标志
2C(g)达到平衡的标志
A.A、B、C的浓度不再随时间的变化而变化
B.单位时间生成n molA 同时生成3n molB
C.C生成的速率等于A分解的速率的2倍
D.A、B、C的分子数比为1:2:3
已知:
CH4(g)+2O2(g)=2CO2(g)+2H2O(l)△H=-Q1
2H2(g)+O2(g)=2H2O(g)△H=-Q2
2H2(g)+O2(g)=2H2O(l)△H=-Q3
常温下取体积比为4:1的CH4和H2的混合气体11.2L(标况)经完全燃烧后恢复至常温,放出的热量是
| A.0.4Q1+0.05Q3 | B.0.4Q1+0.05Q2 | C.0.4Q1+0.1Q3 | D.0.4Q1+0.2Q2 |
丙烯酸的结构简式为CH2=CH—COOH,其对应的性质中不正确的是
| A.与钠反应放出氢气 | B.与新制的Cu(OH)2悬浊液反应 |
| C.能与溴水发生取代反应 | D.能发生反应生成高分子化合物 |