(I)多项选择题
下列说法中正确的是 。
A.丙烯分子中有8个σ键,1个π键
B.在SiO2晶体中,1个Si原子和2个O原子形成2个共价键
C.NF3的沸点比NH3的沸点低得多,是因为NH3分子间有氢键,NF3只有范德华力
D.NCl3和BC13分子中,中心原子都采用sp3杂化
E.SO3与CO32-互为等电子体,SO3是极性分子
(II)人类在使用金属的历史进程中,经历了铜、铁、铝之后,第四种将被广泛应用的金属被科学家预测是钛(Ti),它被誉为“未来世纪的金属”。试回答下列问题:
(1)Ti元素在元素周期表中的位置是第________周期第________族;其基态原子的电子排布式为________。
(2)在Ti的化合物中,可以呈现+2、+3、+4三种化合价,其中以+4价的Ti最为稳定。偏钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构示意图如右图所示,它的化学式是 ,其中Ti4+的氧配位数为 ,Ba2+的氧配位数为 ,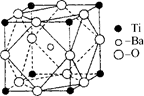
(3)常温下的TiCl4是有刺激性臭味的无色透明液体,熔点-23.2℃,沸点136.2℃,所以TiCl4是 晶体。
4)已知Ti3+可形成配位数为6的配合物,其空间构型为正八面体,如下图1所示,我们通常可以用下图2所示的方法来表示其空间构型(其中A表示配体,M表示中心原子)。配位化合物[Co(NH3)4Cl2]的空间构型也为八面体型,它有 种同分异构体。
(Ⅲ)
(1)已知过氧化氢分子的空间结构如右图所示,分子中氧原子采取 杂化。
(2)R是1~36
号元素中未成对电子数最多的原子。R3+在溶液中存在如下转化关系:
R3+  R(OH)3
R(OH)3  [R(OH)4]-
[R(OH)4]-
①基态R原子的价电子排布式为 ;
②[R(OH)4]-中存在的化学键是 。
A.离子键 B.极性键 C.非极性键 D.配位键
一个课外兴趣小组对某只含Cu、Fe的合金成分含量进行分析(装置见图)。
方法:按图示取a g的Cu、Fe合金和纯铜做为电极,电解液里是含足量的Cu2+离子。接通电源进行实验,一直通电到Cu、Fe合金刚好全部溶解时为止。实验结果是:发现在通电实验过程中两电极均无气体产生,纯铜电极上质量增加19.2g,电解液的质量减少0.8g。请回答:
(1)写出电极反应:阳极;
阴极。
(1)该合金中Cu和Fe的物质的量之比是_________________________。
(3)若另取该合金a g把该Cu、Fe合金与足量的稀硝酸反应后,在溶液中再加入NaOH,能得到的最大沉淀量是________ _g。
银锌电池广泛用作各种电子仪器的电源,其电极分别是Ag2O和锌,电解液为KOH溶液。电池反应是:Ag2O+Zn+H2O="2Ag" +Zn(OH)2,根据上述判断:
(1)原电池的正极是__________,负极是__________。
(2)原电池电极反应式为:负极_______________,正极______________。
(3)工作时原电池负极附近溶液的pH__________ (填“增大”、“不变”、“减小”)。
由氢气和氧气反应生成1mol水蒸气放热241.8KJ。
(1)写出该反应的热化学方程式_______________________。
(2)若1g水蒸气转化成液态水时放热2.444KJ,则反应H2(g) + 1/2O2(g) ==H2O(l)的
△H=______________kJ· 。
。
以下是依据一定的分类标准,对某些物质与水反应的情况进行分类的分类图。请根据你所学的知识,按要求填空:
(1)上述物质的分类方法是;
(2)根据物质与水反应的情况,分成A、B组的分类依据是(选择字母填空,下同),由A组分成C、D组的依据是(填字母)。
a.与水反应后溶液的酸碱性 b.与水反应的剧烈程度 c.是否发生氧化还原反应
(3)F组的物质是(填化学式)。
(4)A组中的酸性氧化物与B组中的某物质反应可用作呼吸面具或潜水艇中氧气的来源,其反应方程式为。
分析下列反应:5KCl + KClO3 + 3H2SO4 = 3Cl2↑+ 3K2SO4 + 3H2O,据此作答:
(1)标出该反应中电子的转移方向和数目:
5KCl + KClO3 + 3H2SO4 = 3Cl2↑+ 3K2SO4 + 3H2O
(2)该反应的氧化剂是。
(3)该反应的氧化产物与还原产物的质量比是。
(4)当反应生成0.3 mol Cl2时,则转移的电子的物质的量是。