为了证明有关物质的性质,某同学设计了如图所示的装置。当打开旋塞C,使A中液体与H中搁板上的固体B相遇时,即有气体产生,并发现D中的蜡烛慢慢熄灭;关闭C打开E时,则看到G中的蜡烛燃得更亮。请回答下列问题:
⑴请写出下列有关仪器的名称:A D
⑵请写出上图装置中有关仪器内盛放的物质的名称:A中 ,固体B ,固体F
⑶用化学方程式表示F中发生的有关反应(用双线桥表示其中之一反应的电子转移方向和数目).
、
(4)、写出H中反应的离子方程式
(本题包括2个小题,共18分)
19.某淡黄色的颗粒状固体,其化学性质比较活泼,在通常状况下能跟许多物质发生化学反应。例如:它与CO2反应时,只生成了Na2CO3和O2,它与稀盐酸反应时,只生成了NaCl、H2O和O2。上课时,老师做了如下实验:
a.取少量的淡黄色的颗粒状固体投入到盛有少量水的试管中,可观察到产生了一种无色无味的气体;
b.再向试管中滴加几滴酚酞试液,可观察到烧杯中溶液变红。
根据实验现象,回答下列问题:
(1)淡黄色的颗粒状固体中一定含有元素。你做出这个判断的理由是。
(2)实验a中产生的气体,可用法收集。
(3)同学们对实验a中产生的气体的组成看法不一,提出了以下几种假设:
①该气体是CO;②该气体是H2。
请你推测该气体还可能是(写化学式)。
(4)设计一个实验,证明你在(3)中的推测(写出简要操作步骤,反应现象和结论)。
| 操作步骤 |
|
| 反应现象 |
|
| 结论 |
现有失去标签的两瓶无色溶液:氯化钠溶液和稀盐酸。某化学探究小组打算用物理和化学两种方法加以区别。请回答:
(1)化学方法在不选用酸碱指示剂、pH试纸的情况下,按表中方法一(示例)填写。所选试剂须属于不同物质类别(单质、氧化物、酸、碱、盐、有机物等)。
| 所选试剂 |
判别方法 |
|
| 方法一 |
锌 |
取少量样品分别与锌反应,有气体产生的是稀盐酸,没有的是氯化钠溶液。 |
| 方法二 |
||
| 方法三 |
(2)物理方法同学小王使用了酒精灯和玻璃棒两种仪器,就把这两种无色溶液区分开了。请你猜测一下他的做法:
操作方法:
判断方法:
[化学——选修2:化学与技术](15分)草酸(乙二酸)可作还原剂和沉淀剂,用于金属除锈、织物漂白和稀土生产。一种制备草酸(含2个结晶水)的工艺流程如下:
回答下列问题:
(1)CO和NaOH在一定条件下合成甲酸钠、甲酸钠加热脱氢的化学反应方程式分别为、。
(2)该制备工艺中有两次过滤操作,过滤操作②的滤液是和,滤渣是。
(3)工艺过程中③和④的目的是。
(4)有人建议甲酸钠脱氢后直接用硫酸酸化制备草酸。该方案的缺点是产品不纯,其中含有的杂质主要是____________________。
(5)结晶水合草酸成品的纯度用高锰酸钾法测定。称量草酸成品0.250 g溶于水,用0.050 0 mol·L-1的酸性KMnO4溶液滴定,至浅粉红色不消褪,消耗KMnO4溶液15.00 mL,反应的离子方程式为;列式计算该成品的纯度。
某研究性学习小组对Zn跟一定量的浓硫酸反应生成的气体产物进行探究。
【提出假设】:小组同学经过分析讨论认为生成气体可能含H2和SO2。
【设计实验方案,验证假设】主要包括两个环节:
Ⅰ.验证SO2,实验装置如图所示;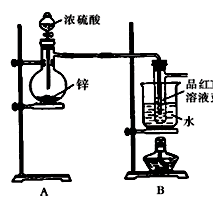
Ⅱ.检验产物中含有H2,实验内容将由B部分导出的气体依次通过装置
C、D、E、F、G。Ⅱ中装置C、D、E、F、G的信息如下表所示:
| 仪器标号 |
C |
D |
E |
F |
G |
| 仪器 |
洗气瓶 |
洗气瓶 |
硬质玻璃管,加热 |
干燥管 |
干燥管 |
| 仪器中所加物质 |
NaOH溶液 |
浓硫酸 |
CuO粉末 |
试剂X |
无水CaCl2固体 |
试回答下列问题:
(1)小组同学认为生成气体中含H2的理由是;
(2)盛放锌粒的仪器名称是;
(3)B部分装置的目的是验证SO2并探究SO2与品红作用的可逆性,实验的操作及主要现象是;
(4)①装置D、G的作用依次是、;
②E中发生反应的化学方程式是;
③试剂X是。
工业上以粗食盐(含有少量Ca2+、Mg2+杂质)、氨、石灰石等为原料,可以制备Na2CO3 。其过程如下图所示。
请回答:(1)在处理粗盐水的过程中,可加入石灰乳和纯碱作为沉淀剂,则所得滤渣的成分除过量的沉淀剂外还有___________________________________。
(2)将CaO投入含有大量的NH4C1的母液中,能生成可循环使用的NH3,该反应的化学方程式是__________________________________。
(3)向饱和食盐水中首先通入的气体是_______________________,过程III中生成NaHCO3晶体的反应的化学方程式是_________________________________________________________。
(4)碳酸钠晶体失水的能量变化示意图如下:
Na2CO3·H2O(s)脱水反应的热化学方程式是。
(5)产品纯碱中常含有NaCl。取ag混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得bg固体。则该产品中Na2CO3的质量分数是。
(6)熔融Na2CO3可作甲烷-空气燃料电池的电解质,该电池负极的反应式是_________________。