下图是苯和溴的取代反应的实验装置图,其中A为具有支管的试管改制成的反应容器,在其下端开了一个小孔,塞好石棉绒,再加入少量的铁屑粉。填写下列空白:
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应。写出A中发生反应的化学方程式(有机物写结构简式): ,反应类型:属于________反应;
(2)试管C中苯的作用是 。反应开始后,观察D和E两试管,看到的现象是D E 。
(3)反应2min~3min后,在B中的氢氧化钠溶液里可观察到的现象是 。
(4)在上述整套装置中,具有防倒吸作用的仪器有 (填字母)。
(5)苯还可以与氢气反应,写出反应方程式 ,反应类型:属于_______反应。
重铬酸钠Na2Cr2O7·2H2O俗称红矾钠,是一种重要的无机盐产品,可作氧化剂,在印染、颜料、电镀、医药等工业方面有广泛的用途。某化学兴趣小组设计实验测定市场上的红矾钠中Na2Cr2O7的质量分数,其步骤如下:
I.称取Wg红矾钠,溶于酸配成l00mL溶液;
Ⅱ.用cmol·L-1的标准KMnO4酸性溶液滴定20.00mL一定浓度的FeSO4溶液,消耗KMnO4溶液20.00rnL;
Ⅲ.取20.00mL Na2Cr2O7溶液,用上述FeSO4溶液滴定,达到滴定终点时,消耗24.00mLFeSO4溶液;
查阅资料知:Cr相对原子质量为52
Cr2O2-7具有强氧化性,在酸性条件下易被还原为Cr3+
回答下列问题:
(1)Na2Cr2O7与FeSO4的反应离子方程式为.
(2)步骤Ⅱ中的滴定过程选用(填“酸式”或“碱式”)滴定管。
(3)已知:MnO-4+5Fe2++8H+==Mn2++5Fe3++4H2O,此红矾钠中Na2Cr2O7的质量分数的表达式为。
(4)判断下列操作对Na2Cr2O7的质量分数测定结果的影响(填“偏高”、“偏低”或“无影响”):
①步骤Ⅲ中的滴定过程,滴定终点读数时俯视读数;
②配制c mol·L-1的KMnO4标准溶液时,转移时有少量溶液洒出。
(5)有同学提出FeSO4有很强的还原性,在空气中易被氧化而变质,因此对测定结果会造成影响,请你分析后指出,如果FeSO4变质,对测定结果的影响是(填“偏高”、“偏低”或“无影响”)。
(12分)50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。
回答下列问题:
(1)烧杯间填满碎木屑的作用是__________________________。
(2)环形玻璃搅拌棒能否用环形铜质搅拌棒代替? (填“能”或“不能”),其原因是_______________________________。
(3)为什么要用0.55 mol·L-1的氢氧化钠溶液?
____________________________________________________;
实验中若改用60 mL 0.50 mol·L-1的盐酸与50 mL 0.55 mol·L-1的氢氧化钠溶液进行反应,与上述实验相比,所测得的中和热 (填“相等”或“不相等”)。
有甲、乙两位同学想利用下列装置及化学试剂,对实验室制取并收集氨气的实验进行改进。
化学试剂:①NH4Cl固体②浓氨水③固体NaOH
(1)甲同学想方便快速制取少量氨气,应选择的装置是_________ (填序号)。
选用试剂是_________(填序号) ,选用上述试剂制氨气的理由是___________________。
(2)乙同学建议,把教材中实验室制取氨气的收集装置由大试管改为集气瓶且瓶口向上收集氨气,并确保不污染环境,若用这种排气法收集氨气,请在图Ⅱ的方框内画出其气体收集装置和尾气吸收装置,标出所用试剂(自选)名称。
实验室要配制1mol/L的稀硫酸250mL,回答下列问题:
(1)需要98%密度为1.84g/cm3的浓硫酸mL(1分)
(2)配制时,必须使用的仪器有 (填代号)(1分)
①烧杯 ②100 mL量筒 ③20 mL量筒④1000 mL容量瓶⑤250 mL容量瓶⑥托盘天平(带砝码)⑦ 玻璃棒;还缺少的仪器是 。(1分)
玻璃棒;还缺少的仪器是 。(1分)
(3)配制时,该实验两次用到玻璃棒,其作用分别是、。(各1分)
(4)配制过程中出现以下情况,对所配溶液浓度有何影响(填“偏高”“偏低”
“不影响”)
①没有洗涤烧杯和玻璃棒。 。(1分)
②如果加水超过了刻度线,取出水使液面恰好到刻度线。 。(1分)
③容量瓶没有干燥。 (1分)
已知非金属单质硫(S)是淡黄色固体粉末,难溶于水。为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题: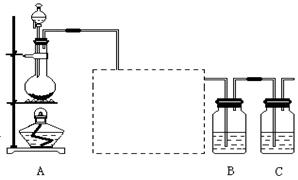
(1) 装置A的分液漏斗中盛装的试剂是 ,烧瓶中加入的试剂是。
,烧瓶中加入的试剂是。
(2)画出虚线框内的实 验装置图,并注明所加试剂,说明装置的作用。
验装置图,并注明所加试剂,说明装置的作用。
(3) 装置B中盛放的试剂是(此空选填下列所给试剂的代码),实验现象为,化学反应方程式是,该反应属于四种基本反应类型中的反应。
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
(4) 还有哪些事实能够说明氯元素的非金属性比硫元素的非金属性强(试举一例)。。
(5)装置C中盛放烧碱溶液,目的是吸收反应后剩余的气体,防止污染空气。在该反应中,Cl元素的化合价既有升高又有降低,即在反应中Cl元素的原子既能获得电子也能失去电子,能否说氯元素既具有金属性又具有非金属 性?简述你的理由。
性?简述你的理由。