向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水, 难溶物溶解得到深蓝色的透明溶液。下列对此现象说法正确的是
难溶物溶解得到深蓝色的透明溶液。下列对此现象说法正确的是
| A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 |
| B.在[Cu(NH3)4] 2+离子中,Cu2+给出孤对电子,NH3提供空轨道 |
| C.向反应后的溶液加入乙醇,溶液没有发生变化 |
D.沉淀溶解后,将生成深蓝色的配合离子[Cu(NH3)4] 2+ 2+ |
下列方程式书写正确的是
A.CO32-的水解方程式:CO32-+2H2O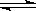 H2CO3+2OH- H2CO3+2OH- |
B.H2SO3的电离方程式H2SO3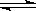 2H++SO32- 2H++SO32- |
C.HCO3- 在水溶液中的电离方程式:HC O3-+H2O O3-+H2O H3O++CO32- H3O++CO32- |
D.CaCO3的电离方程式:CaCO3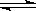 Ca2++CO32- Ca2++CO32- |
下列说法不正确的是
| A.属于放热和熵增加的反应,就更易自发进行 |
| B.溶液在稀释过程中,溶液中的阴、阳离子浓度都减小 |
| C.对某可逆反应而言,其平衡常数K值越大,反应物的转化率也越大 |
| D.向2.0 mL浓度均为0.1 mol/L的KCl、KI混合溶液中滴加1~2滴0.01 mol/L AgNO3溶液,振荡,沉淀呈黄色,说明AgCl的Ksp比AgI的Ksp大 |
升高温度,下列数据不一定同时增大的是
| A.化学反应速率v | B.弱酸的电离平衡常数Ka |
| C.化学平衡常数K | D.水的离子积常数Kw |
空气是人类生存所必需的重要资源。为改善空气质量而启动的“蓝天工程”得到了全民的支持。下列措施不利于“蓝天工程”建设的是
| A.推广使用燃煤脱硫技术,防治SO2污染 |
| B.实施绿化工程,防治扬尘污染 |
| C.研制开发燃料电池汽车,消除机动车尾气污染 |
| D.加大石油、煤炭的开采速度,增加化石燃料的供应量 |
中和滴定是一种操作简单,准确度高的定量分析方法。实际工作中也可利用物质间的氧化还原反应、沉淀反应进行类似的滴定分析,这些滴定分析均需要通过指示剂来确定滴定终点,下列对几种具体的滴定分析(待测液置于锥形瓶内)中所用指示剂及滴定终点时的溶液颜色的判断不正确的是( )
| A.用标准酸性KMnO4溶液滴定Na2SO3溶液以测量其浓度:KMnO4——紫红色 |
| B.利用“Ag++SCN-===AgSCN↓”原理,可用标准KSCN溶液测量AgNO3溶液浓度:Fe(NO3)3——红色 |
C.利用“2Fe3++2I-===I2+2Fe2+”, 用FeCl3溶液测量KI样品中KI的百分含量: 用FeCl3溶液测量KI样品中KI的百分含量:淀粉——蓝色 |
| D.利用OH-+H+===H2O来测量某盐酸溶液的浓度时:酚酞——浅红色 |