氮是地球上极为丰富的元素
(1)Li3N晶体中氮以N3-的形式存在,基态N3-的电子排布式为____________;
(2)X离子中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶体结构如右图所示。X的元素符号是______,X离子与N3-形成的化合物化学式为______。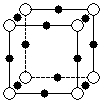
(3)水是生命之源,它与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是_____(请用相应的编号填写)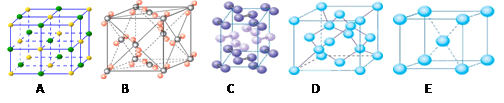
(4)在冰晶体中,每个水分子与相邻的4个水分子形成氢键,已知冰的升华热是51 kJ/mol,除氢键外,水分子间还存在范德华力(11 kJ/mol),则冰晶体中氢键的“键能”是_________kJ/mol;
硫及其部分化合物的转化关系如图所示。
(1)通常状况下硫单质的颜色为_________。
(2)SO2可以使品红溶液褪色,说明SO2具有_________(填“漂白性”或“氧化性”)。
(3)化合物A的化学式为__________。
(4)反应⑤的离子方程式为___________________________。
(5)反应④中,当32g Cu完全反应时,被还原的H2SO4的物质的量为________mol。
某些铁、铝制品的表面常生成一层氧化物,其主要成分分别是氧化铁、氧化铝。两种氧化物均能与盐酸反应,生成的两种盐的化学式分别为_____________、____________。向这两种盐的溶液中分别滴加足量氢氧化钠溶液,可观察到:其中一种溶液中的现象是先产生白色沉淀,然后白色沉淀逐渐消失则该溶液为_____________溶液;另一种溶液中的现象是______(填序号)。
①产生白色沉淀
②产生红褐色沉淀
③产生白色沉淀,迅速变成灰绿色,最后变成红褐色
印刷电路板是由塑料和铜箔复合而成,刻制印刷电路时要用FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2,其反应的化学方程式如下:Cu+ 2FeCl3═ CuCl2 + 2FeCl2
(1)指出上述反应中氧化剂是__________,还原剂是__________。
(2)使用过的腐蚀液会失效,但还可以回收利用,其中有一步需要将Fe2+转化为Fe3+,下列试剂能实现上述变化的是_______(填序号)。
| A.氯气 | B.铁 | C.盐酸 | D.稀硫酸 |
在Cl2、NO、SO2、NO2、NH3五种气体中,与空气相遇能立即变色的是_________;
常用于自来水杀菌、消毒的是________;能用向下排空气法收集的是__________;溶于水后能生成强酸的是_________。
已知在柑橘、柠檬等水果中含有柠檬酸,且已知柠檬酸中只含C、H、O三种元素。 现对该物质进行研究,以测得其结构。
(1)取柠檬酸19.2 g,在氧气中完全燃烧,产生CO2和H2O分别为26.4 g和7.2 g,进行质谱分析,可获得柠檬酸的相对分子质量为192,通过计算,可获得柠檬酸的分子式为____________。
(2)利用__________________分析可知柠檬酸分子中含有—COOH和—OH。
(3)再利用核磁共振氢谱分析发现有4个吸收峰,其峰面积之比为4∶2∶1∶1。综合以上信息,写出柠檬酸的结构简式__________________________________。