回收再利用锗产品加工废料,是生产GeO2的重要途径,其流程如下图。
(1)Ge2+与氧化剂H2O2反应生成Ge4+,写出该反应的离子方程式:
▲ 。
(2)蒸馏可获得沸点较低的GeCl4,在此过程中加入浓盐酸的原因是:
▲ 。
(3)GeCl4水解生成GeO2·nH2O,此过程用化学方程式可表示为: ▲ 。温度对GeCl4的水解率产生的影响如右图所示。为控制最佳的反应温度,实验时可采取的措施为 ▲ 。(填字母)
A.用冰水混合物 B.49℃水浴 C.用冰盐水
(4)根据下表1 中不同pH下二氧化锗的溶解率,结合Ge在元素周期表中的位置及“对角线”法则,分析GeO2溶解率随pH 变化的原因 ▲ ,用离子方程式表示pH>8时GeO2溶解率增大可能发生的反应 ▲ 。
表1 不同pH下二氧化锗的溶解率
| pH |
4 |
5 |
6 |
7 |
8 |
9 |
| 溶解率/% |
47.60 |
32.53 |
11.19 |
5.27 |
1.96 |
8.85 |
已知:A是石油裂解气的主要产物之一,其产量常用于衡量一个石油化工发展水平的标志。下列是有机物A~G之间的转化关系: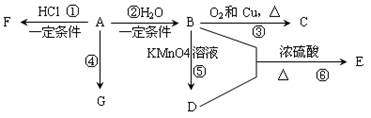
请回答下列问题:
(1)A的官能团的名称是________________;C的结构简式是________________;
(2)E是一种具有香味的液体,由B + D→的反应方程式为:________________,该反应类型是_______________;
(3)G是一种高分子化合物,其链节是______________;
(4)比赛中,当运动员肌肉挫伤或扭伤时,随队医生即对准受伤部位喷射物质F(沸点12.27OC)进行应急处理。写出由A制F的化学反应方程式:_____________________,决定F能用于冷冻麻醉应急处理的性质是___________________。
从海水中可以获得淡水、食盐,并可提取镁和溴等物质。
(一)海水淡化的方法主要有 (只填一种)。
(二)从海水中提取溴和镁的流程如下图所示: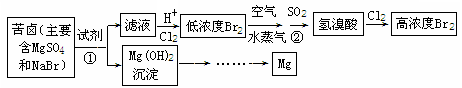
(1)提取Br2时,第一次通入Cl2后发生反应的离子方程式是
②中SO2表现 (填“氧化”或“还原”)性;第二次通入Cl2后,要提取Br2还要进行的操作为 。
(2)为了实现对镁离子的富集,①中加入的足量试剂是 (填化学式);
请从节约能源,提高金属镁的纯度分析,以下最适宜的冶炼的方法是 (填字母)。
A.Mg(OH)2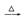 MgO MgO  Mg Mg |
B.Mg(OH)2 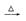 MgO MgO  Mg Mg |
C.Mg(OH)2 无水MgCl2 无水MgCl2 Mg Mg |
D.Mg(OH)2 MgCl2(溶液) MgCl2(溶液) Mg Mg |
将检验下列溶液所用试剂的序号填入相应的括号中。
①检验葡萄糖溶液();
②检验淀粉溶液();
③检验蛋白质溶液()。
| A.KI溶液 |
| B.碘水 |
| C.浓硝酸 |
| D.稀硫酸 |
E.新制的Cu(OH) 2悬浊液
(12分) ①~⑩是元素周期表中的十种元素:
| 主族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
| 2 |
① |
② |
③ |
||||
| 3 |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
||
| 4 |
⑨ |
⑩ |
回答下列问题:
(1)某同学对下列性质进行了对比,其中正确的是 。
A.原子半径:⑩>⑨>⑦
B.离子半径:⑨>④>⑦
C.非金属性:③>②>⑥
D.单质的熔点:④>⑨>⑩>⑧
E.单质的氧化性:③>⑦>⑧
(2)用合适的化学用语回答:
金属性最强的元素离子结构示意图为 ,
常温下呈液态的氢化物的结构式为 。
溶于水后溶液显碱性的氢化物的电子式为 。
(3)在上述元素中,②、⑧元素形成的气态氢化物可以相互反应,该反应的化学方程式为 ;⑨、⑤元素形成的最高价氧化物的水化物可以相互反应,该反应的离子方程式为 。
(1)目前出现的“不粘锅”,其秘密就是表面有一种叫做“特氟龙”的涂层,实际上就是号称”塑料王”的聚四氟乙烯,试写出四氟乙烯单体合成“特氟龙”的化学方程式和其反应类型。
反应 类型
(2)请写出硬脂酸甘油酯制肥皂的化学方程式和反应类型
反应 类型
(3)请写出苯与浓硝酸反应的化学方程式和反应类型
反应 类型