某化学小组采用类似乙酸乙酯的装置(如下图)用环己醇制备环己烯。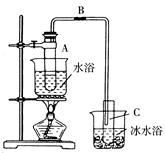
已知:
| |
密度(g/cm3) |
熔点(℃) |
沸点(℃) |
溶解性 |
| 环己醇 |
0.96 |
25 |
161 |
能溶于水 |
| 环己烯 |
0.81 |
-103 |
83 |
难溶于水 |
(1)制备粗品
将12.5 mL还已醇加入试管A中,再加入1 mL浓硫酸摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是______________,导管B除了导气外还具有的作用是_______________
②试管C置于冰水浴中的目的是__________________
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在__________ 层(填“上”或“下”),分液后用__________(填入编号)洗涤。
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按图装置蒸馏,冷却水从________ 口进入。
蒸馏时要加入生石灰,目的是_______________________
③收集产品时,控制的温度应在__________左右,实验
制得的环己烯精品质量低于理论产量,
可能的原因________ (填序号)
a.蒸馏时从70 ℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度。
(1)滴定
①用______式滴定管盛装0.1000 mol/L盐酸标准液,锥形瓶中装有25.00mL待测烧碱溶液。上图表示某次滴定时50 mL滴定管中前后液面的位置。请将用去的标准盐酸的体积填入②表空格中。
②有关数据记录如下:
| 滴定序号 |
待测液体积(mL) |
所消耗盐酸标准液的体积(mL) |
||
| 滴定前 |
滴定后 |
消耗的体积 |
||
| 1 |
25.00 |
0.50 |
25.95 |
25.45 |
| 2 |
25.00 |
|||
| 3 |
25.00 |
6.00 |
31.55 |
25.55 |
(2)根据所给数据,计算出烧碱样品的物质的量浓度(注意保留合适的有效数字)。
c(NaOH) = _____________。
(3)读数时,若滴定前仰视,滴定后俯视,则会使最终测定结果_________。(填“无影响”、“偏高”、“偏低”)
两套如图所示装置,各盛有2g锌粒(颗粒大小相同)分别加入40ml 1mol/L和40ml 4mol/L的硫酸,比较二者收集10ml H2时所用的时间。
(1)当收集到10mL H2时,哪个实验所耗时间较长?为什么?
_________________________________________________________________________________
(2)活塞外移的情况是_______________。
| A.均匀外移 | B.先快后慢 | C.先慢后快 | D.先慢后快然后又逐渐减慢 |
你选择的理由是___________________________________________________________。
同学想通过下图所示装置(夹持装置已略去)进行实验,研究推断SO2与Na2O2反应的产物。
回答下列问题:
(1)装置B的作用___________________________________________________。
装置D除了吸收过量的SO2外还有什么作用___________________________。
(2)如何检验反应中是否有O2生成______________________________________。
(3)假如Na2O2已反应完全,为确定C中固体产物的成分,甲设计如下实验:
得出结论:产物是Na2SO4.
该方案是否合理____________(填是或否),理由是_____________________-。
海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
请填写下列空白:
(1)步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,步骤③和步骤⑥该步骤的实验操作名称分别是是。
(2)步骤①灼烧海带时,除需要三脚架、泥三角外,还需要用到的实验仪器是
| A.烧杯 | B.表面皿 | C.坩埚 | D.酒精灯 E.干燥器 |
(3)步骤⑥是从含碘苯溶液中分离出单质碘和回收苯,还需经过蒸馏,指出下列实验装置中的错误之处。
①
②
③
(4)进行上述蒸馏操作时,使用水浴的原因是①;
最后晶态碘在②里聚集。
(5)步骤④反应的离子方程式是。
步骤④中的转化还可以Cl2或双氧水(H2O2),请分别写出反应的离子方程式:,
。
(6)步骤⑤中,某学生选择用苯来提取碘的理由是。
(7)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:。
色谱分析法是现代分离实验技术中的一种,试回答下列问题:
(1)已知两种有机色素A 与B混合在一起,经测定知A的极性比B强,则下列说法正确的是_________
A. 用溶解过滤法,B不溶A溶于水
B. 用重结晶法,A在水中的溶解度比B大
C. 用蒸馏法,因为A的熔沸点高
D. 用纸层析法,丙酮为展开剂,下端为A,上端为B
(2)纸层析法的原理是_________
A.萃取原理 B. 毛细现象 C. 蒸馏原理 D. 极性相似相溶原理 E.过滤
(3)在用纸层法进行层析操作时,为什么不能让滤纸上的试样点接触展开剂?__________。