NA表示阿伏加德罗常数的值,下列说法正确的是
| A.250C时,pH=2的1.0L H2SO4溶液中含有的H+数目为0.02NA |
| B.0.5mol雄黄(,结构如右图)含有NA个S - S键 |
| C.将含有lmolFeCl3溶质的饱和溶液加人沸水中可以得到1 mol Fe(OH)3胶粒 |
| D.向含有FeI2的溶液中通入适蛩氣气,当有1molFe2+被氧化时,该反应转移电子的数目至少为3NA |
【原创】某有机物常用于制备液晶材料,结构简式为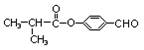 ,则下列说法正确的是
,则下列说法正确的是
| A.该有机物的分子式为C12H8O3 |
| B.该有机物可以发生水解反应、加成反应、氧化反应、还原反应 |
| C.该有机物的一溴代物有4种 |
| D.该物质属于芳香烃 |
X、Y为短周期元素,X位于第IA族,X与Y可形成化合物X2Y,下列说法不正确的是
| A.两元素还可能形成原子个数比为1:1的化合物 |
| B.X与Y的简单离子可能具有相同电子层结构 |
| C.X的原子半径一定大于Y的原子半径 |
| D.X2Y可能是离子化合物,也可能是共价化合物 |
【改编】制备食用碘盐(KIO3)原理之一为:I2+2KClO3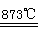 Cl2+2KIO3,下列说法正确的是
Cl2+2KIO3,下列说法正确的是
| A.向KClO3溶液中滴加AgNO3溶液得到白色AgCl沉淀 |
| B.反应过程中I2置换出Cl2,由此可推断非金属性I>CI |
| C.KClO3和KIO3均属于离子化合物,都只含有离子键 |
| D.制备KIO3的反应中氯元素被还原 |
化学与生活、社会密切相关,下列说法正确的是
| A.合金的许多性能优于其组成成分,如硬度都会增大,熔点都会升高 |
| B.要除去衣服上的顽固污渍,可将衣服泡在漂白液中 |
| C.硅是地壳中含量位居第二的元素,其中玛瑙、光导纤维的主要成分为SiO2 |
| D.工业上获得大量的乙烯、丙烯、丁二烯的方法是石油裂化 |
室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:
| 实验 编号 |
c(HA)起始浓度/(mol·L-1) |
c(KOH)起始浓度/(mol·L-1) |
反应后溶液的pH |
| ① |
0.1 |
0.1 |
9 |
| ② |
x |
0.2 |
7 |
下列判断不正确的是
A.实验①反应后的溶液中:c(K+)>c(A-)>c(OH-)>c(H+)
B.0.1 mol·L-1HA的溶液中由水电离出的 c(H+)=1×10-13 mol/L
C.实验②反应后的溶液中:c(A-)+c(HA)>0.1 mol/L
D.实验②反应后的溶液中:c(K+)=c(A-)>c(OH-)=c(H+)