(10分)恒温时,将2molA和2molB气体投入固定容积为2L密闭容器中发生反应:2A(g) + B(g)  xC (g) + D(s),10s时,测得A的物质的量为1.7mol,C的反应速率为0.0225mol·L—1·s—1;40s时反应恰好处于平衡状态,此时B的转化率为20%。请填写下列空白:
xC (g) + D(s),10s时,测得A的物质的量为1.7mol,C的反应速率为0.0225mol·L—1·s—1;40s时反应恰好处于平衡状态,此时B的转化率为20%。请填写下列空白:
(1)x = 
(2)从反应开始到40s达平衡状态,A的平均反应速率为
(3)平衡时容器中B的体积分数为
(4)该温度下此反应的平衡常数表达式为 数值是
(5)下列各项能表示该反应达到平衡状态是
A.消耗A的物质的量与生成D的物质的量之比为2∶1
B.容器中A、B的物质的量 n(A)∶n(B) =2∶1
C.气体的平均相对分子质量不再变化
D.压强不再变化
E.气体密度不再变化
(6)在相同温度下,若起始时c(A)="5" mol·L-1,c(B)=6mol·L-1,反应进行一段时间后,测得A的浓度为3mol·L-1,则此时该反应是否达到平衡状态 (填“是”与“否”),此时v(正) v(逆)(填“大于”“小于”或“等于”)。
将饱和FeCI3溶液滴入沸水中可以得到的氢氧化铁胶体,请回答下列问题:
(1)该氢氧化铁胶体粒子直径在 之间。
(2)将其装入U型管中,用石墨电极接通直流电,通电一段时间后,发现阴极附近的颜色 ,这个现象说明 ,胶体的这种性质称为电泳。
(3)向氢氧化铁胶体中滴入过量稀硫酸,现象是
(4)除了以上性质外,氢氧化铁胶体还具有的性质有 。
(5)写出制备氢氧化铁胶体的化学方程式 。
(l)一块金属钠露置于空气中,可以观察到如下现象:
银白色→变灰暗→变白色→出现液滴→白色固体
请写出变化过程中可能发生的反应的化学方程式:
(2)一块金属钠直接空气中加热充分反应。①可以观察到的现象为发生反应的化学方程式为 ;②若将反应后的产物投入到水槽中,则发生反应的化学方程式为 ,此反应中的氧化剂是 ,被氧化的元素是
A、B、C、D四种短周期元素,A元素的一种同素异形体是自然界硬度最大的单质,C与A同主族,C元素的原子序数是B的2倍,工业上以D元素的单质与石灰乳为原料制造漂白粉。按要求回答下列问题:
(1)B的原子结构示意图为 ;镁条在气体B中燃烧生成的物质是 (填化学式);
(2)A的非金属性强于C,请用一个化学反应方程式表示_______________;
(3)写出元素D的单质与石灰乳制漂白粉的化学方程式 。
向20 mL某物质的量浓度的AlCl3溶液中滴入2 mol·L-1NaOH溶液时,得到的Al(OH)3沉淀质量与所滴加的NaOH溶液的体积(mL)关系如图所示,试回答下列问题: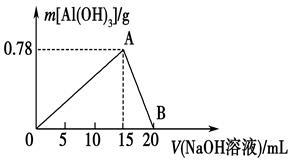
(1)图中A点表示的意义是_________________________。
(2)图中B点表示的意义是_________________________。
(3)上述两步反应用总的离子方程式可表示为:__ ____。
(4)若所得Al(OH)3沉淀0.39 g,则此时用去NaOH溶液的体积为______________。
(1)铜既能与稀硝酸反应.也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为: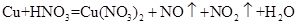 (未配平)
(未配平)
①硝酸在该反应中的作用是__________________,
②19.2g Cu被硝酸完全溶解后,若得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是__________________。
(2)①已知白磷和氯酸溶液可发生如下反应:
P4 + HClO3 + = HCl + H3PO4
配平上述反应方程式。
②白磷有毒,有实验室可采用CuSO4溶液进行处理,其反应为:
11P4 + 60CuSO4 + 96H2O = 20Cu3P + 24 H3PO4 + 60 H2SO4
在该反应中30molCuSO4可氧化P4的物质的量是 。